
-

生物通官微
陪你抓住生命科技
跳动的脉搏
高分辨率成像揭示细胞内寄生虫的宿主细胞逃逸机制:从分子动态到靶向治疗新策略
【字体: 大 中 小 】 时间:2025年10月09日 来源:BIOspektrum
编辑推荐:
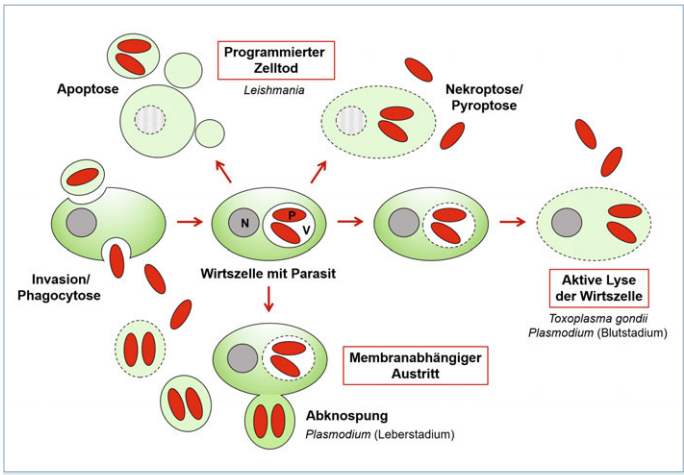
本期推荐德国研究团队通过STED、STORM、Expansion Microscopy等高分辨率成像技术,系统解析了疟原虫(Plasmodium)、弓形虫(T. gondii)和利什曼原虫(Leishmania)等病原体利用程序性细胞死亡、主动裂解及膜包被非裂解三种策略逃逸宿主细胞的动态过程。该研究首次整合多组学与实时成像数据,发现疟原虫肝期逸出依赖关键蛋白酶、弓形虫通过CRISPR-Cas9筛选鉴定出两个逸出调控蛋白,为抗寄生虫药物研发提供了新靶点。
 生物通微信公众号
生物通微信公众号