
-

生物通官微
陪你抓住生命科技
跳动的脉搏
基于CRISPR/Cas9技术在人iPSC来源巨噬细胞中发现TNFRSF1A基因内含子1具有增强子活性的证据
【字体: 大 中 小 】 时间:2025年10月09日 来源:Scientific Reports 3.9
编辑推荐:
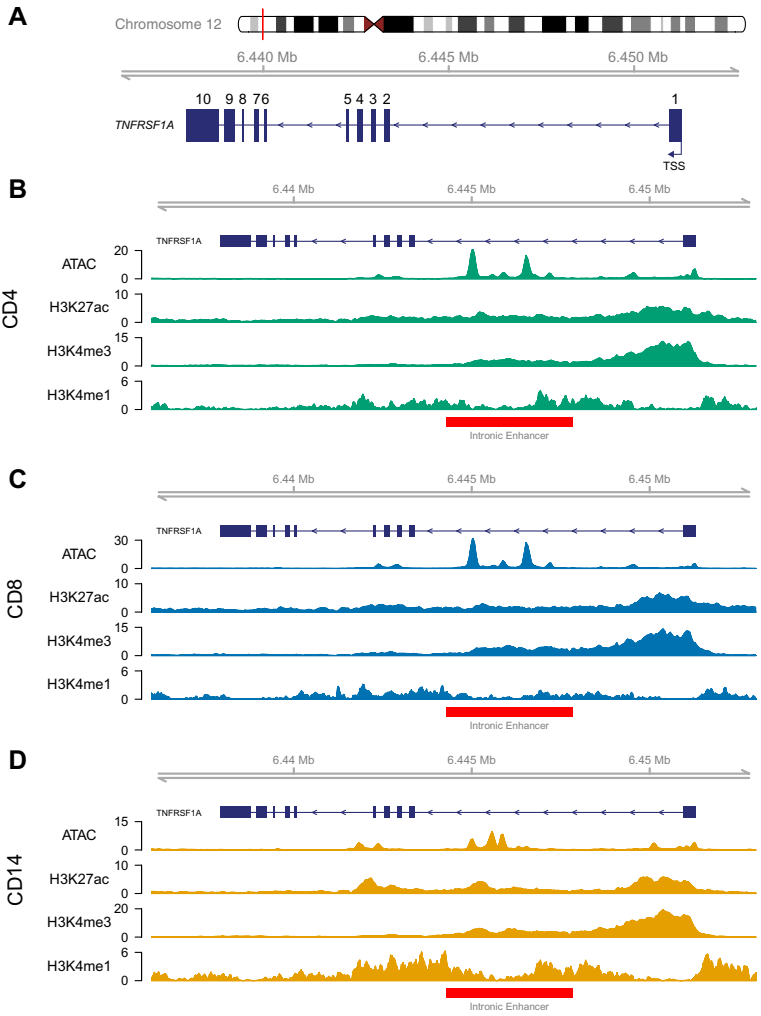
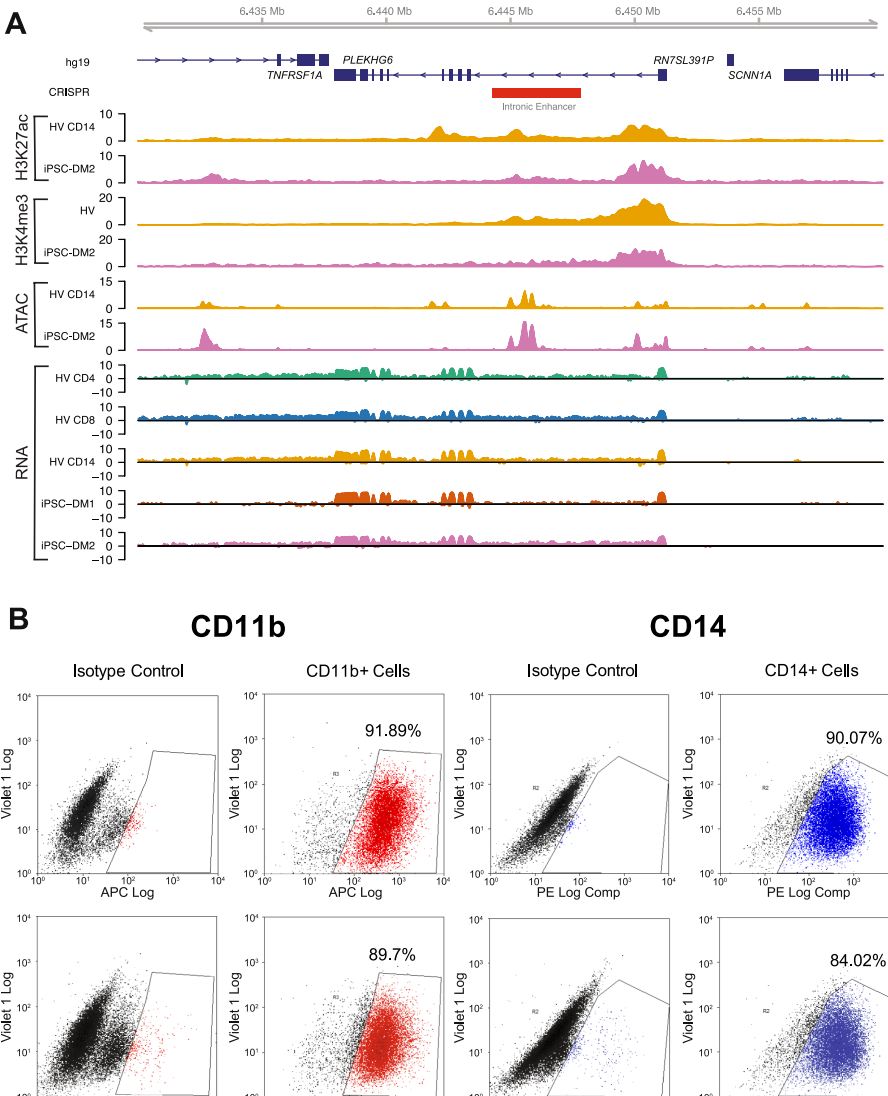
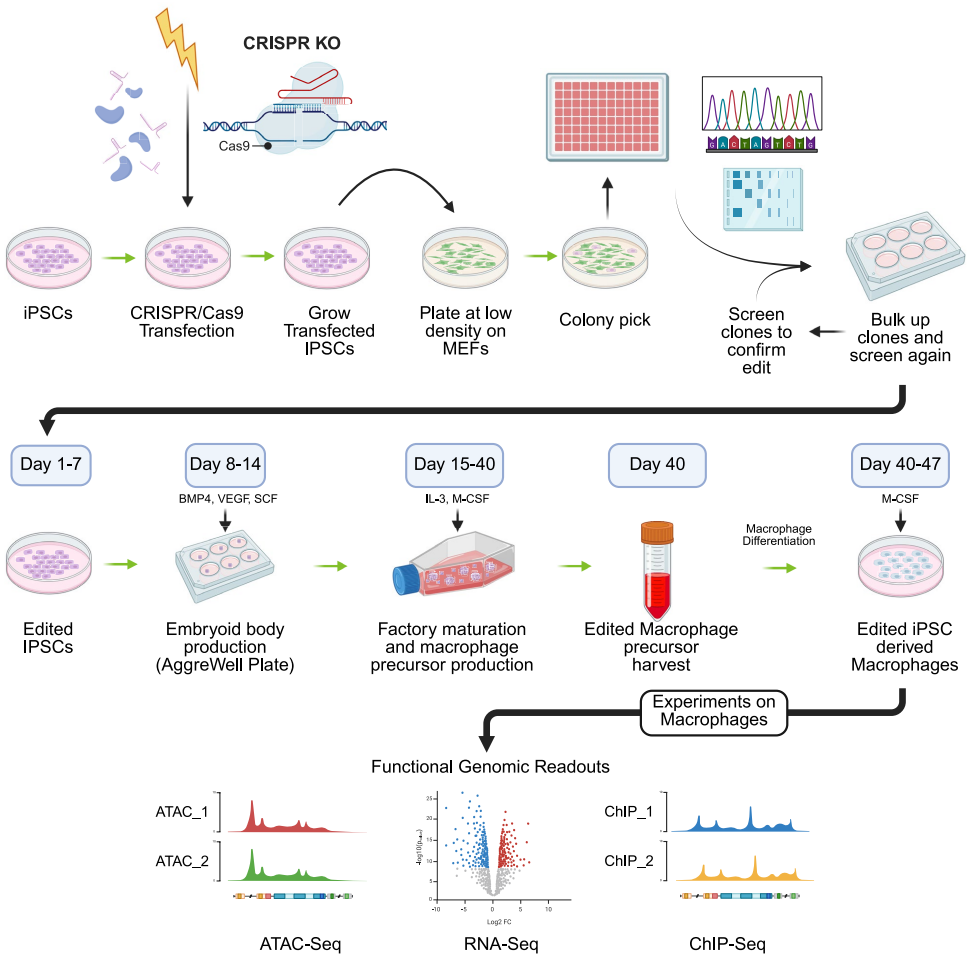
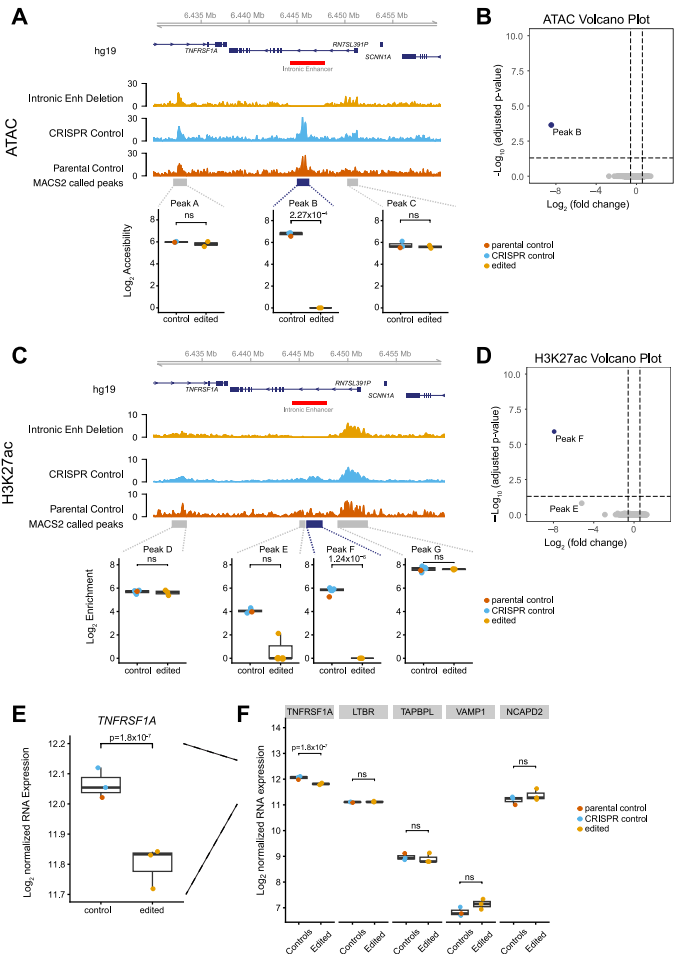
本研究针对TNFRSF1A基因调控机制不清的问题,利用CRISPR/Cas9技术在人诱导多能干细胞(iPSC)来源的巨噬细胞中开展功能基因组学研究,发现该基因第一内含子区域存在一个功能性增强子。通过多组学分析(ATAC-Seq、ChIP-Seq、RNA-Seq)证实该增强子缺失会导致TNFRSF1A表达显著下调,为解析自身免疫疾病GWAS变异的功能机制提供了重要实验依据。
 生物通微信公众号
生物通微信公众号