
-

生物通官微
陪你抓住生命科技
跳动的脉搏
系统性比较CRISPR-Cas9等位基因编辑技术在耳念珠菌中的应用:揭示线性盒整合不可靠性及环状质粒编辑的高效性
【字体: 大 中 小 】 时间:2025年10月09日 来源:Scientific Reports 3.9
编辑推荐:
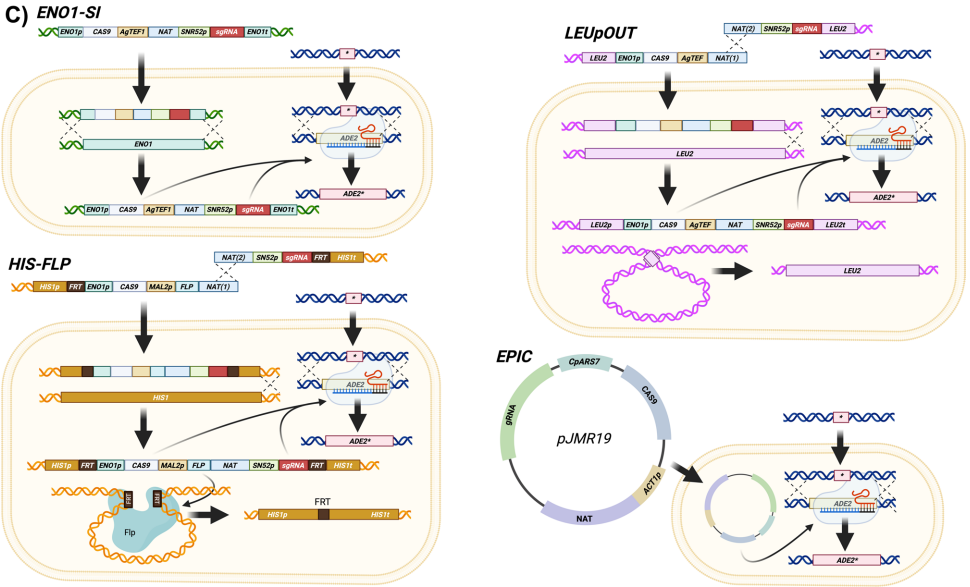
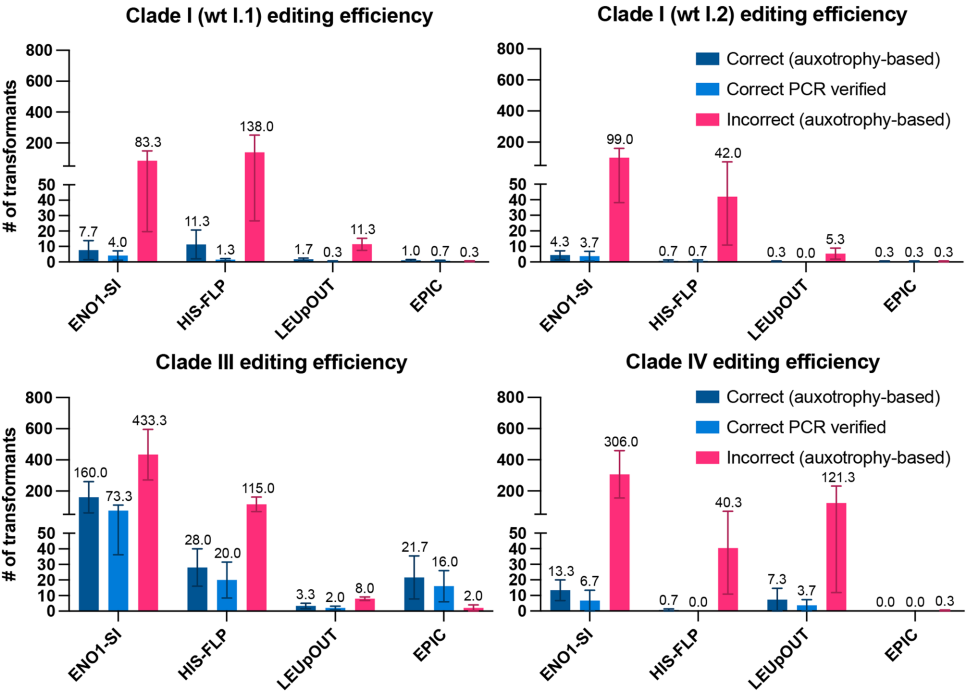
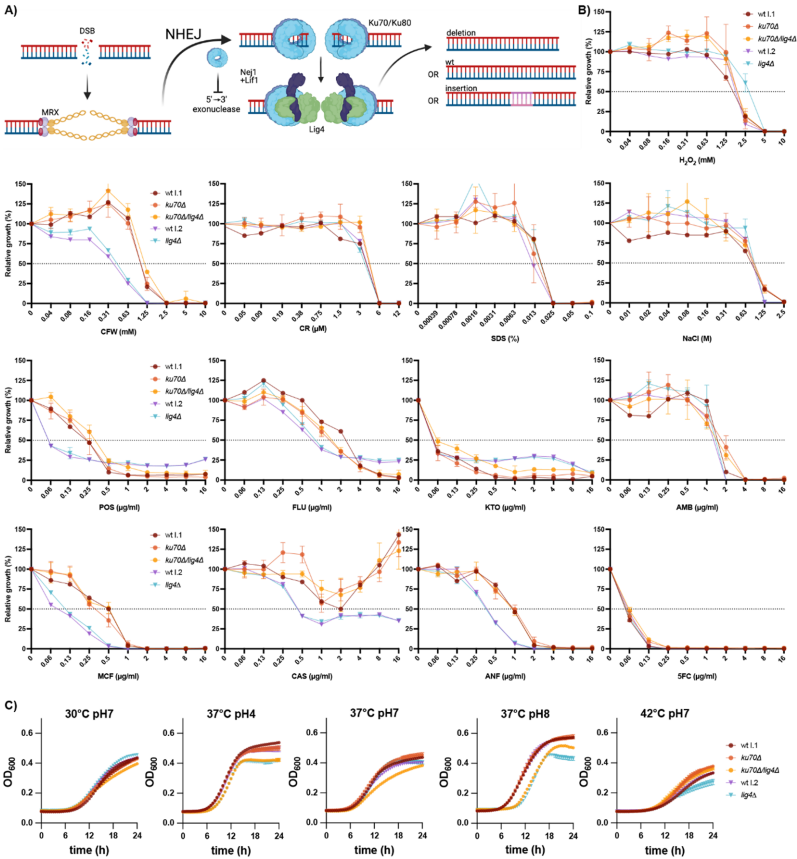
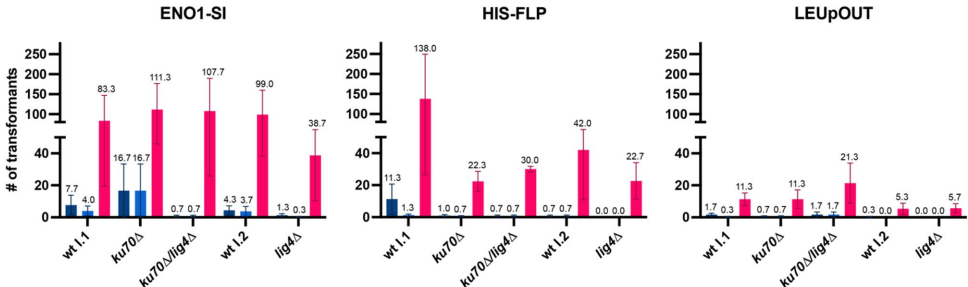
本研究针对新兴病原真菌耳念珠菌(Candida auris)基因组编辑效率低、方法不统一的难题,系统比较了四种CRISPR-Cas9系统(ENO1-SI、LEUpOUT、HIS-FLP和EPIC)的编辑效率。研究发现,基于线性盒整合的系统普遍存在外源DNA片段异常整合问题,而基于环状质粒的EPIC系统虽转化子数量较少,但编辑准确率最高(平均41.9%)。研究还发现敲除非同源末端连接(NHEJ)通路关键基因KU70和LIG4并未提升编辑效率。该研究为耳念珠菌分子生物学研究提供了可靠工具选择依据,并警示基因组编辑中需严谨验证整合准确性。
 生物通微信公众号
生物通微信公众号