
-

生物通官微
陪你抓住生命科技
跳动的脉搏
mTORC2介导的细胞间相互作用通过促进WNT信号激活调控中内胚层分化
【字体: 大 中 小 】 时间:2025年10月17日 来源:Stem Cell Reports 5.1
编辑推荐:
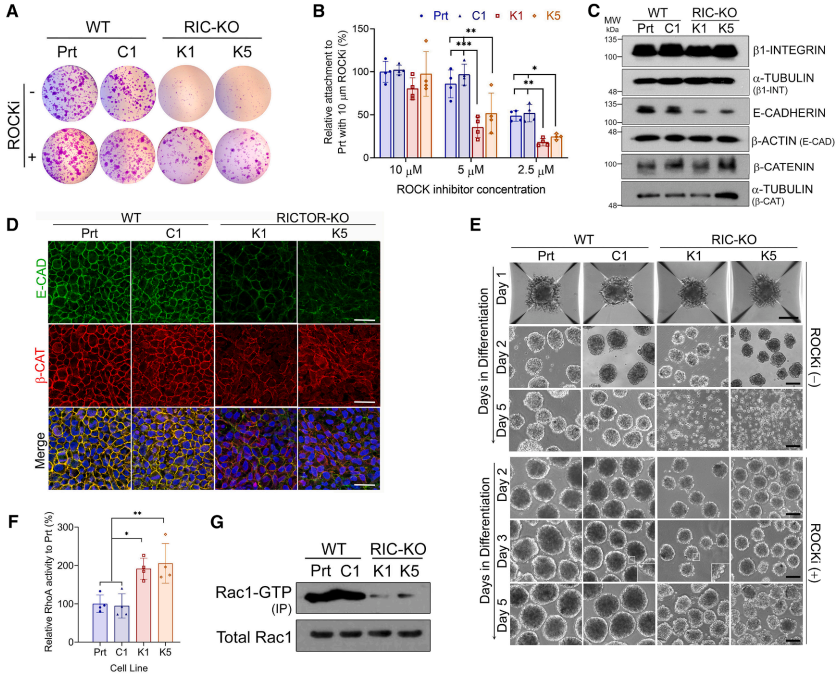
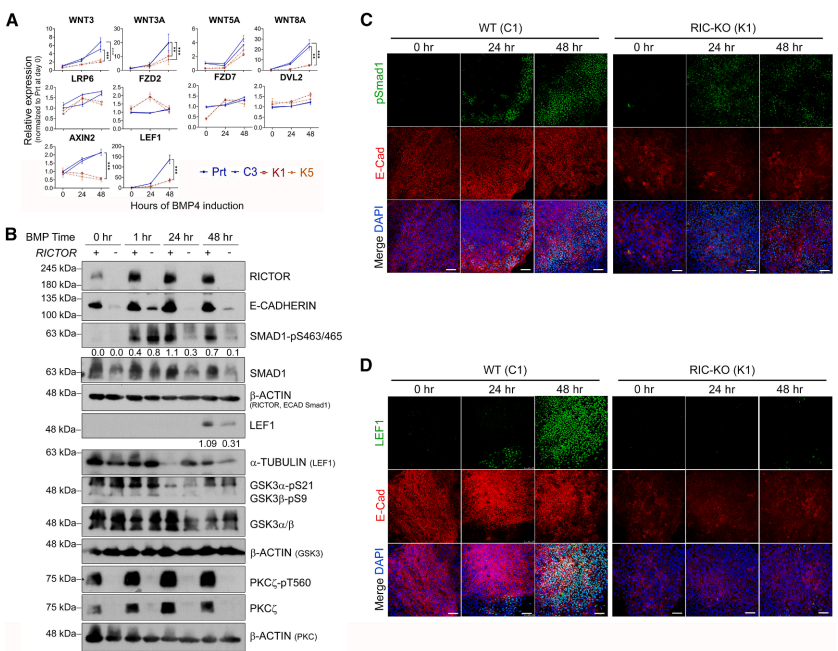
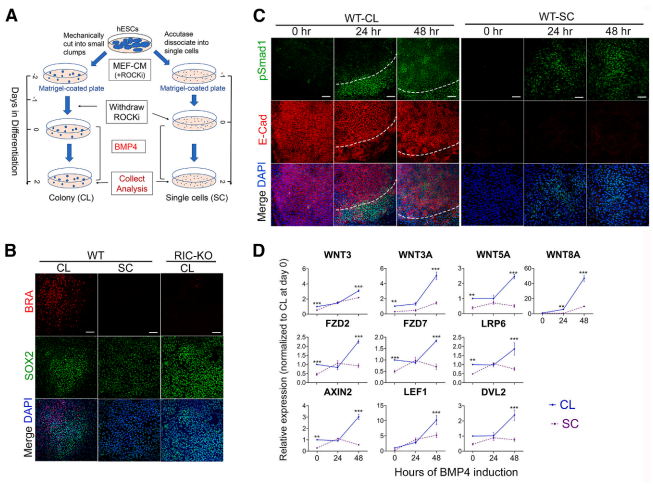
本研究针对mTORC2在早期胚胎发育中的分子机制不明确的问题,通过构建RICTOR基因敲除的人胚胎干细胞模型,发现mTORC2通过调节Rho/Rac信号动态平衡维持细胞黏附,并揭示其缺陷会导致BMP4诱导的WNT信号激活障碍和mesendoderm分化受损。研究首次阐明了mTORC2通过细胞间相互作用调控经典WNT基因表达的新机制,为理解胚胎发育和干细胞命运决定提供了重要见解。




 生物通微信公众号
生物通微信公众号