
-

生物通官微
陪你抓住生命科技
跳动的脉搏
基于crRNA表达的梨火疫病菌基因编辑新方法构建及其在致病机理研究中的应用
【字体: 大 中 小 】 时间:2025年11月15日 来源:Phytopathology Research 3.5
编辑推荐:
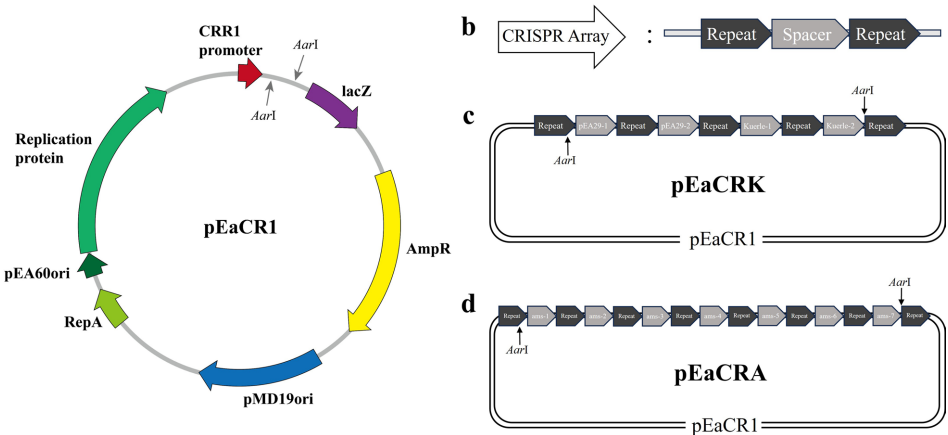
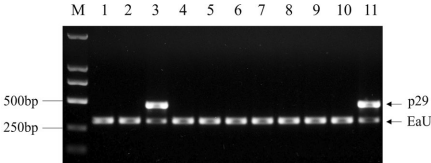
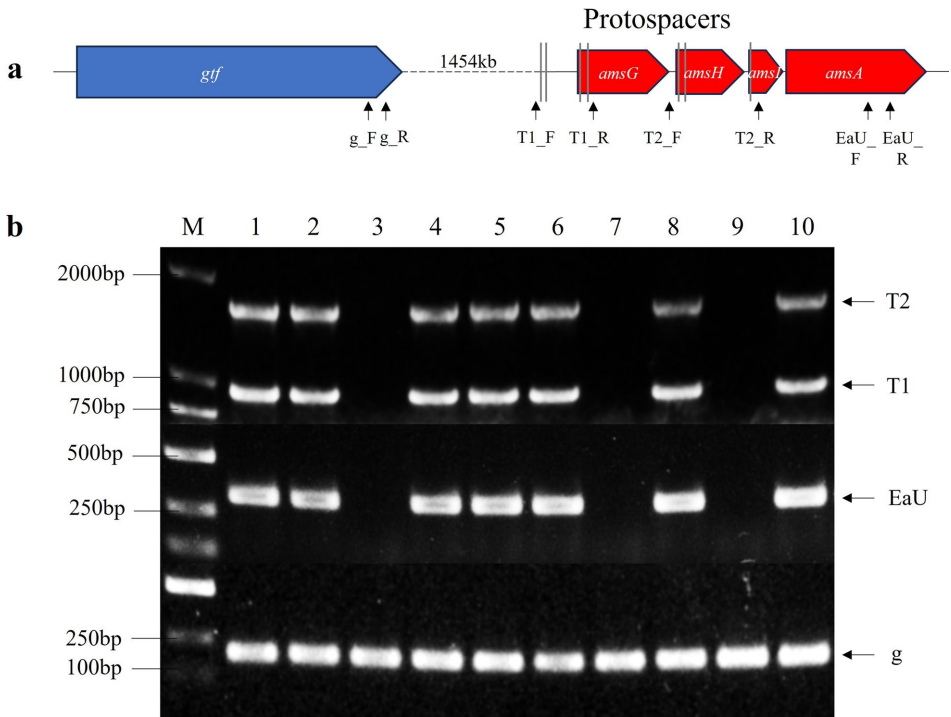
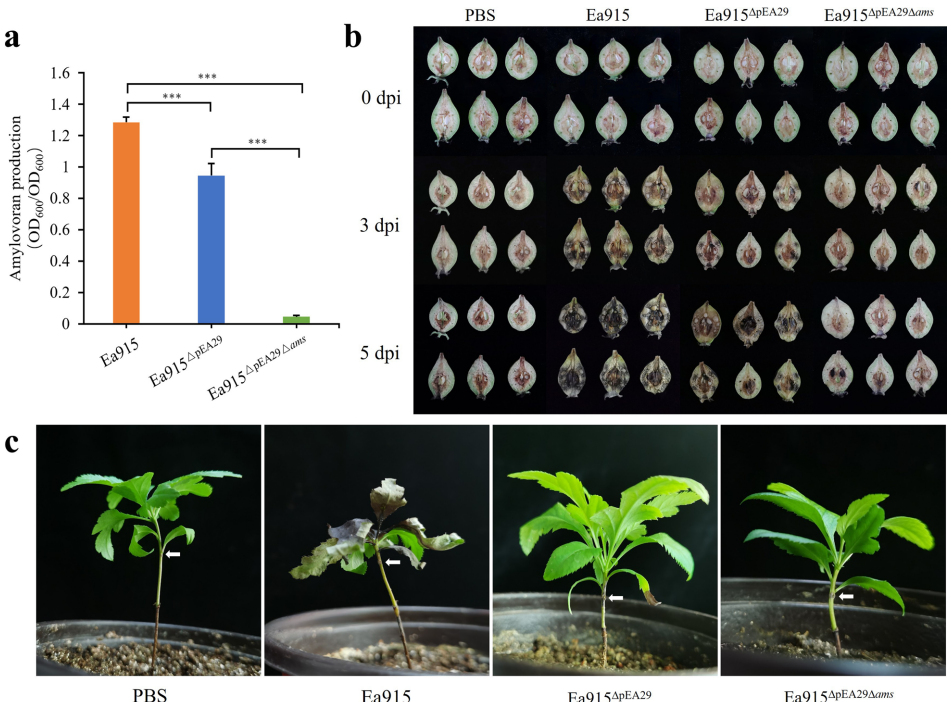
本研究针对梨火疫病菌(Erwinia amylovora)缺乏有效基因组编辑工具的问题,开发了一种基于内源I-E型CRISPR/Cas系统的基因敲除方法。研究人员通过构建crRNA表达质粒,成功实现了pEA29质粒消除和ams操纵子大片段缺失突变体的构建。全基因组测序结果显示该方法能产生33.1-51.5kb的大片段缺失,且未检测到脱靶效应。该方法为梨火疫病菌功能基因组学研究提供了重要技术支撑。

 生物通微信公众号
生物通微信公众号