
-

生物通官微
陪你抓住生命科技
跳动的脉搏
猪δ冠状病毒通过脂滴动态调控病毒感染的分子机制研究
【字体: 大 中 小 】 时间:2025年11月19日 来源:Virology Journal 3.8
编辑推荐:
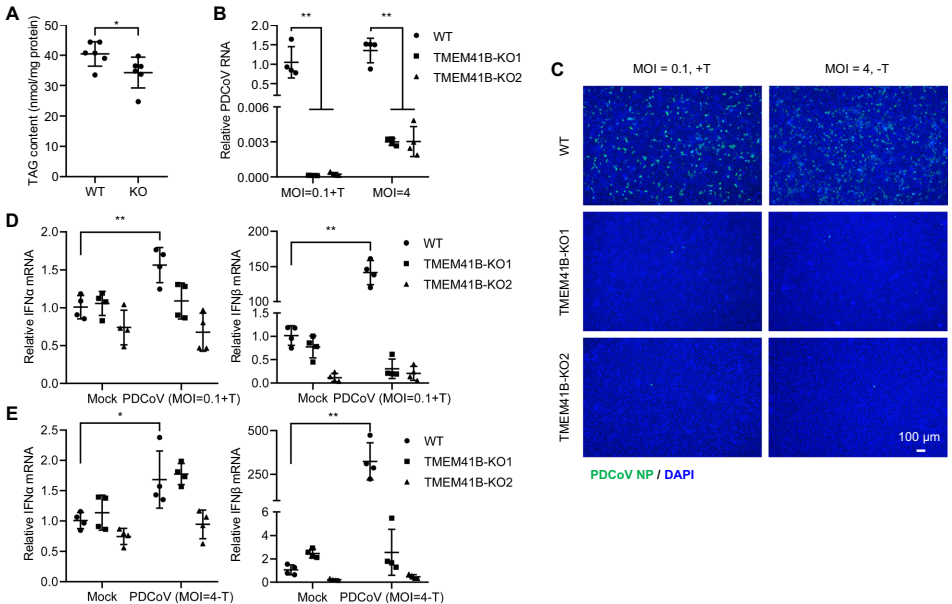
本研究针对猪δ冠状病毒(PDCoV)如何调控宿主细胞脂滴稳态这一关键科学问题,系统揭示了PDCoV感染通过改变脂质代谢相关基因表达促进脂滴积累,而过度积累的脂滴通过增强I/III型干扰素(IFN)反应和内质网(ER)应激发挥抗病毒作用。研究人员进一步发现跨膜蛋白41B(TMEM41B)作为关键调控因子,其缺失导致脂滴形态异常并显著抑制PDCoV感染。该研究为理解冠状病毒与宿主脂代谢互作提供了新视角,为开发广谱抗病毒策略提供了潜在靶点。





 生物通微信公众号
生物通微信公众号