
-

生物通官微
陪你抓住生命科技
跳动的脉搏
靶向AMFR-FAM134B轴调控内质网自噬:克服骨肉瘤缺氧耐受的多功能纳米治疗新策略
【字体: 大 中 小 】 时间:2025年11月19日 来源:Journal of Nanobiotechnology 12.6
编辑推荐:
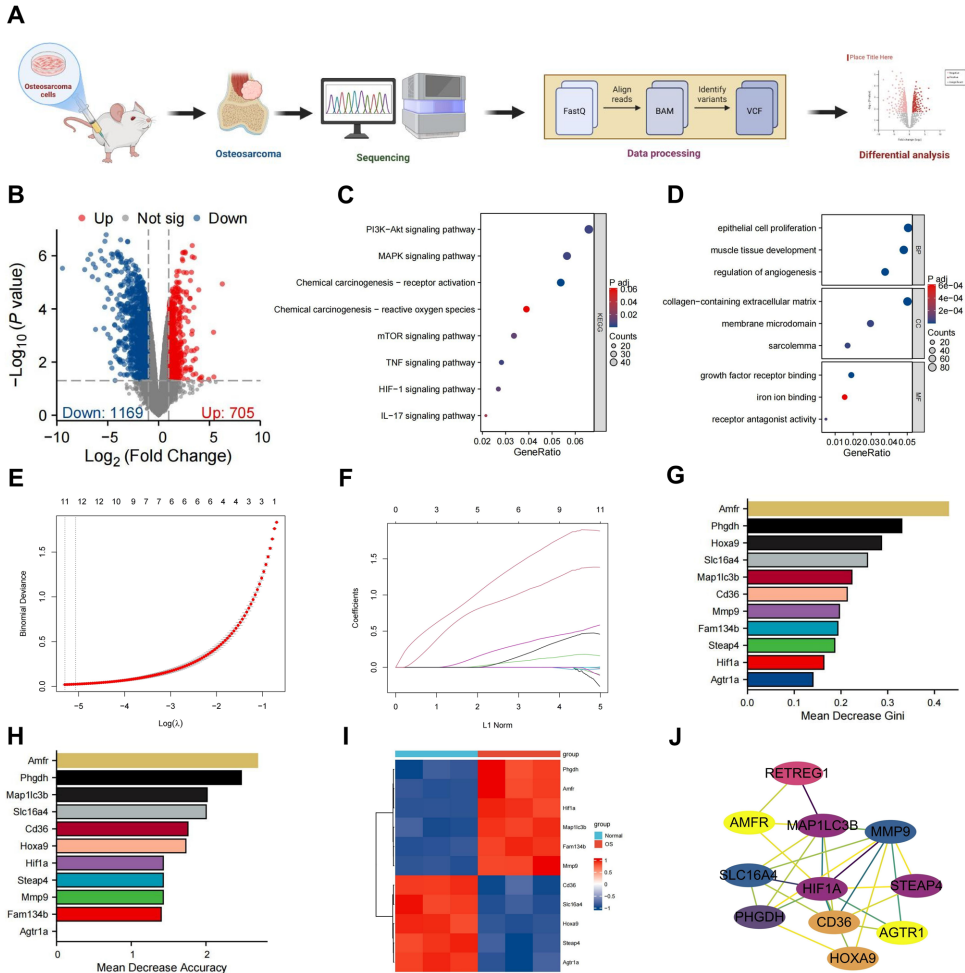
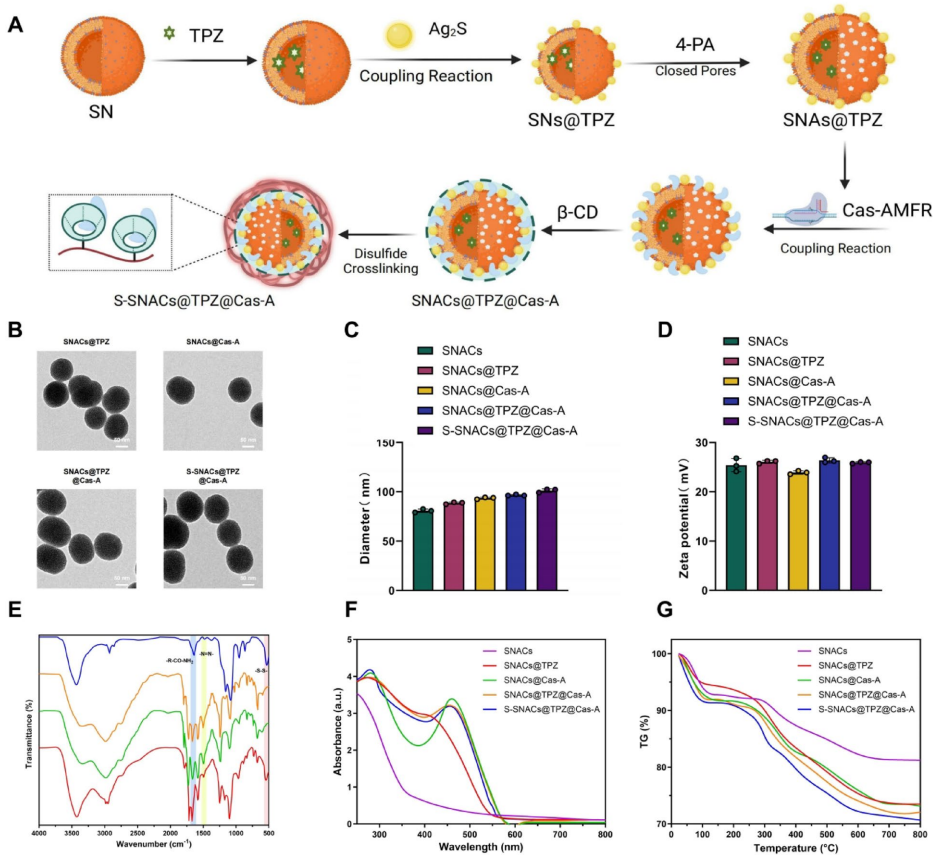
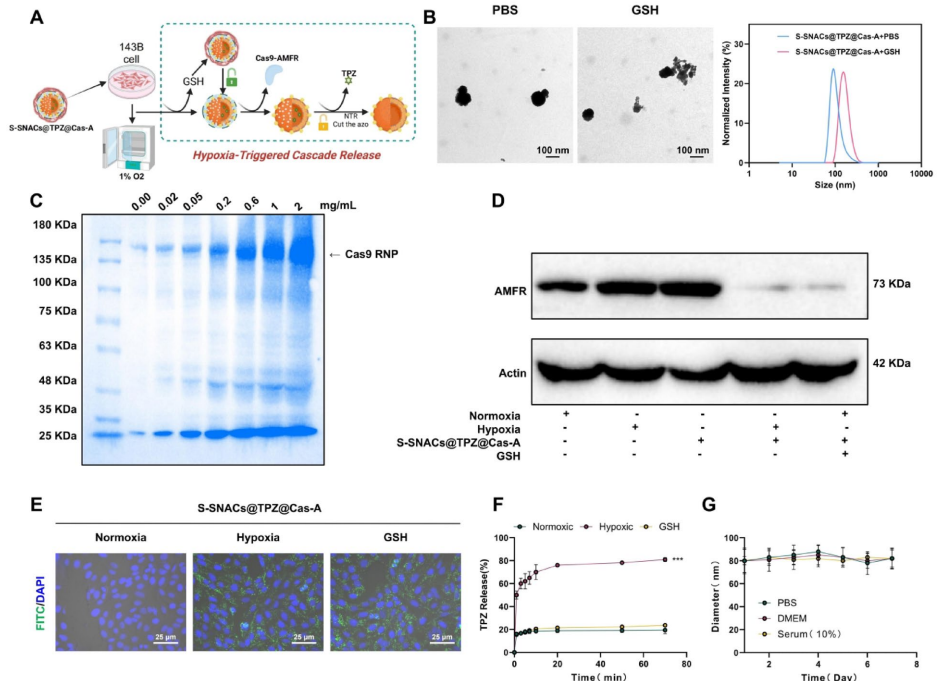
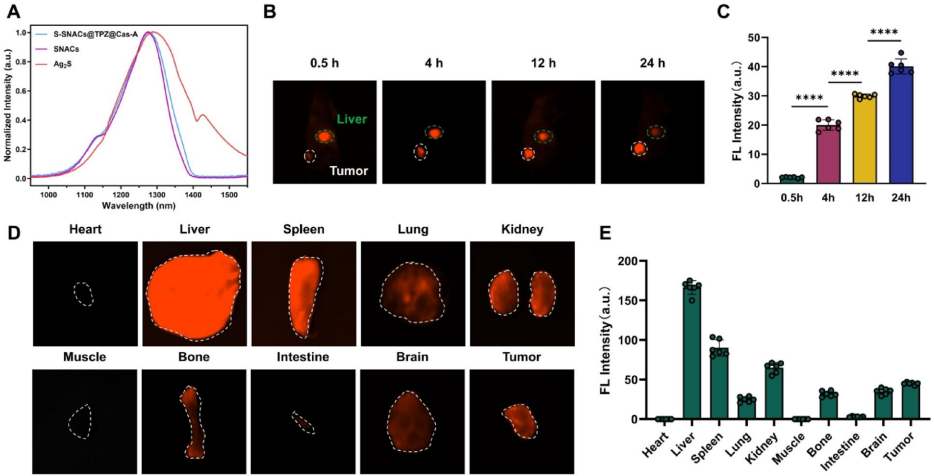
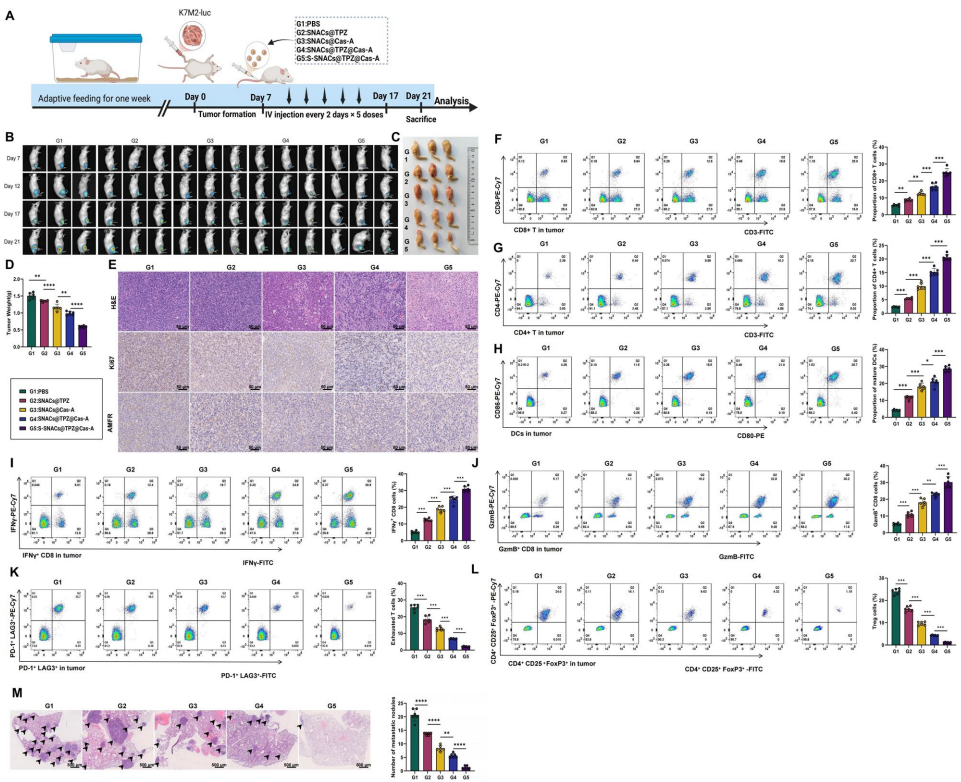
本文推荐一项针对骨肉瘤缺氧耐受机制的治疗策略研究。研究人员发现AMFR介导的FAM134B泛素化在缺氧适应中起关键作用,并开发了S-SNACs@TPZ@Cas-A纳米平台,该平台通过CRISPR-Cas9基因编辑联合替拉扎明(TPZ)药物,有效抑制肿瘤生长、减少肺转移并改善免疫微环境。这项研究为缺氧耐受性肿瘤的精准治疗提供了新思路。

 生物通微信公众号
生物通微信公众号