
-

生物通官微
陪你抓住生命科技
跳动的脉搏
EF1α启动子替代CMV启动子优化CAR-T细胞体外杀伤效价评估:解决IFN-γ/NF-κB通路干扰的精准检测新策略
《Molecular Therapy Methods & Clinical Development》:EF1α, rather than CMV promoter, is suitable for luciferase tag expression in target cells for in vitro cytotoxicity assays of CAR-T cells
【字体: 大 中 小 】 时间:2025年07月30日 来源:Molecular Therapy Methods & Clinical Development 4.6
编辑推荐:
本研究针对CAR-T细胞体外杀伤实验中CMV启动子驱动的荧光素酶(Luc)报告系统因IFN-γ/NF-κB通路激活导致假阳性信号的关键问题,通过多模型对比分析揭示EF1α启动子具有最佳检测一致性,为免疫细胞治疗效价评估提供了标准化解决方案。
在肿瘤免疫治疗领域,CAR-T细胞的杀伤效价评估如同"黑箱测试"――研究者需要精准量化这些工程化免疫细胞摧毁肿瘤靶细胞的能力,但传统检测方法却暗藏玄机。荧光素酶报告系统作为主流检测手段,其原理看似简单:让靶细胞携带发光标签,通过光信号强弱判断存活细胞数量。然而徐州医科大学的研究团队发现,当使用巨细胞病毒(CMV)启动子驱动荧光素酶表达时,CAR-T细胞攻击竟会引发反常现象――随着靶细胞死亡,发光信号不降反升,如同"将死之人的回光返照"。
这一反常现象背后,隐藏着免疫治疗评估体系的重大隐患。CMV启动子含有NF-κB等应激响应元件,当CAR-T细胞分泌干扰素γ(IFN-γ)时,会激活靶细胞内NF-κB信号通路,意外增强CMV启动子活性,导致荧光素酶表达水平与细胞存活数量背道而驰。徐州医科大学癌症研究所的Rui Hou等研究人员通过构建五种不同启动子(EF1α、SFFV、hPGK、CAG、SV40)的荧光素酶报告系统,在三种CAR-T杀伤模型(靶向PDPN的胃癌模型、靶向CD19的白血病模型和靶向Her2的黑色素瘤模型)中展开系统性验证。
研究采用流式细胞绝对计数法作为金标准,结合Pearson相关性分析和Bland-Altman一致性检验等统计方法。关键技术包括:①构建CMV-Luc异常激活的三种CAR-T/靶细胞共培养模型;②通过IFN-γ基因敲除CAR-T细胞(Her2 CAR-TIFN-γ KO)和NF-κB抑制剂(JSH-23)处理验证调控机制;③多启动子报告系统的平行比较与标准化评估。
主要发现如下:
CMV启动子驱动的Luc报告系统不适用于CAR-T细胞杀伤评估
在PDPN CAR-T攻击HGC-27胃癌细胞、CD19 CAR-T攻击Nalm6白血病细胞、Her2 CAR-T攻击B16F10黑色素瘤细胞的三类模型中,CMV-Luc信号均呈现与细胞死亡程度负相关(r<0)。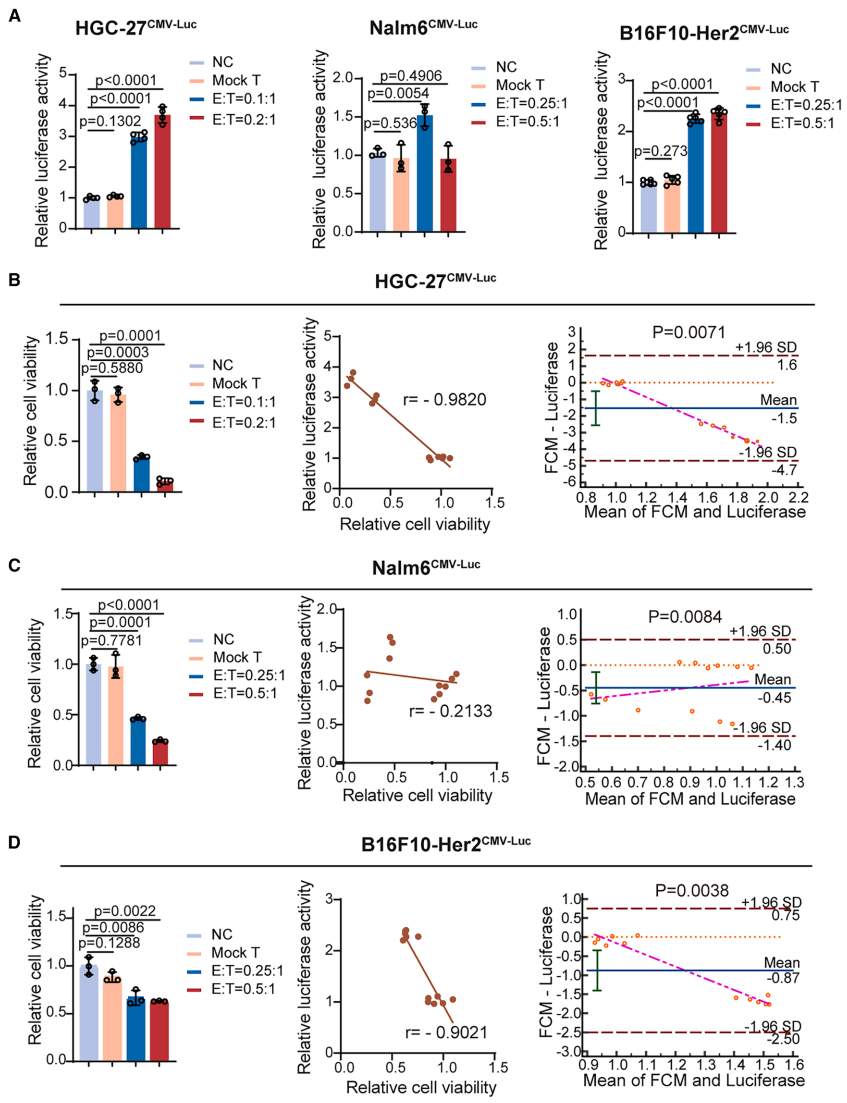
CAR-T细胞通过分泌IFN-γ异常增强CMV启动子活性
IFN-γ敲除的CAR-T细胞(Her2 CAR-TIFN-γ KO)丧失信号增强效应,而外源添加IFN-γ可重现该现象。qPCR证实CAR-T攻击使靶细胞Luc mRNA水平提升2-5倍,且NF-κB抑制剂JSH-23能完全阻断此效应,而CREB抑制剂666-15无效。

EF1α启动子展现最佳检测一致性
在五类启动子横向比较中,EF1α-Luc与流式细胞计数结果的Pearson相关系数最高(r>0.7),且Bland-Altman分析显示最小偏差。尤其在Her2 CAR-T模型中,EF1α是唯一保持正相关趋势的启动子。

这项发表于《Molecular Therapy Methods》的研究确立了启动子选择对CAR-T效价评估的决定性影响:CMV启动子因受免疫微环境调控会产生假阳性信号,而EF1α启动子因其组成型稳定表达特性,能真实反映靶细胞存活状态。该发现不仅为CAR-T产品标准化质控提供关键方法学依据,更警示科研界需重新审视现有报告系统在免疫治疗场景中的适用性――当评估涉及IFN-γ分泌细胞的杀伤实验时,启动子选择可能成为数据可靠性的"阿喀琉斯之踵"。未来研究可基于EF1α启动子构建通用型报告细胞系,推动免疫细胞治疗评估进入"去干扰"的新阶段。
 生物通微信公众号
生物通微信公众号