
-

生物通官微
陪你抓住生命科技
跳动的脉搏
超越单基因变异:基于通路分析探索记忆遗传基础的新范式
《Molecular Neurobiology》:Beyond Single Variants: A Pathway-Based Approach to Explore the Genetic Basis of Memory
【字体: 大 中 小 】 时间:2026年01月16日 来源:Molecular Neurobiology 4.3
编辑推荐:
本研究针对记忆作为复杂性状难以通过传统GWAS识别遗传因素的挑战,提出采用宽松p值阈值结合多维度功能注释的通路分析策略。通过对人类连接组计划中三种记忆测试的基因组数据进行分析,发现在通路层面存在显著重叠,揭示了神经发育、突触传递等关键生物学机制,为深入理解记忆的遗传架构提供了新视角。
记忆是人类认知功能的核心,但揭示其遗传基础却面临巨大挑战。传统研究往往聚焦于寻找单个"记忆基因",然而记忆作为复杂性状,很可能由成千上万个微效遗传变异共同作用形成。这就如同在茫茫星海中寻找特定星座,单靠肉眼观察难以发现规律,需要更先进的观测方法。
在记忆研究领域,存在三个主要瓶颈:首先,记忆具有高度多基因性,每个遗传变异贡献微小,需要超大样本才能检测;其次,记忆本身包含工作记忆、情景记忆等不同类型,不同研究采用的测试方法各异;第三,为获得深度表型数据而牺牲样本规模的研究,往往统计效力不足。这些因素导致既往研究结果难以重复,遗传机制认识支离破碎。
正是在这样的背景下,来自马斯特里赫特大学的研究团队在《Molecular Neurobiology》上发表了一项创新性研究。他们另辟蹊径,不再执着于寻找达到基因组显著性水平的单个变异,而是采用更宽松的p值阈值(p<1×10-5),结合系统的功能注释和通路分析,探索记忆的遗传基础。这种策略类似于从寻找单个亮星转向识别整个星系的结构,有望发现更有生物学意义的模式。
研究团队选择人类连接组计划(HCP)数据集作为验证平台,这个选择颇具匠心。HCP虽然样本量相对有限(n≈1200),但提供了深度的多模态表型数据,包括三种不同类型的记忆测试:Penn-Word言语情景记忆测试、Picture Sequence视觉情景记忆测试以及List Sorting言语工作记忆测试。这种设计使得研究人员能够同时考察不同记忆类型的共享和独特遗传基础。
关键技术方法包括:对HCP队列的基因组数据进行质量控制,使用GCTA工具进行GWAS分析,采用FUMA平台进行变异映射和功能注释,通过Cytoscape进行通路网络可视化,并与GWAS Catalog中的已有研究进行对比验证。
研究人员首先确认了三种记忆测试作为遗传研究对象的合理性。结果显示,Penn-Word测试和Picture Sequence测试的遗传力估计分别为39.1%和42.0%,而List Sorting工作记忆测试的遗传力高达61.7%,均达到中等至高度遗传力水平,支持后续遗传分析的可行性。
表型相关性分析发现,不同记忆测试得分之间虽然存在显著相关,但决定系数(R2)最高仅为0.09(Picture Sequence与List Sorting之间),表明这些测试确实捕获了部分独立认知维度。这一发现印证了记忆的多维度特性,也为分别进行GWAS分析提供了依据。
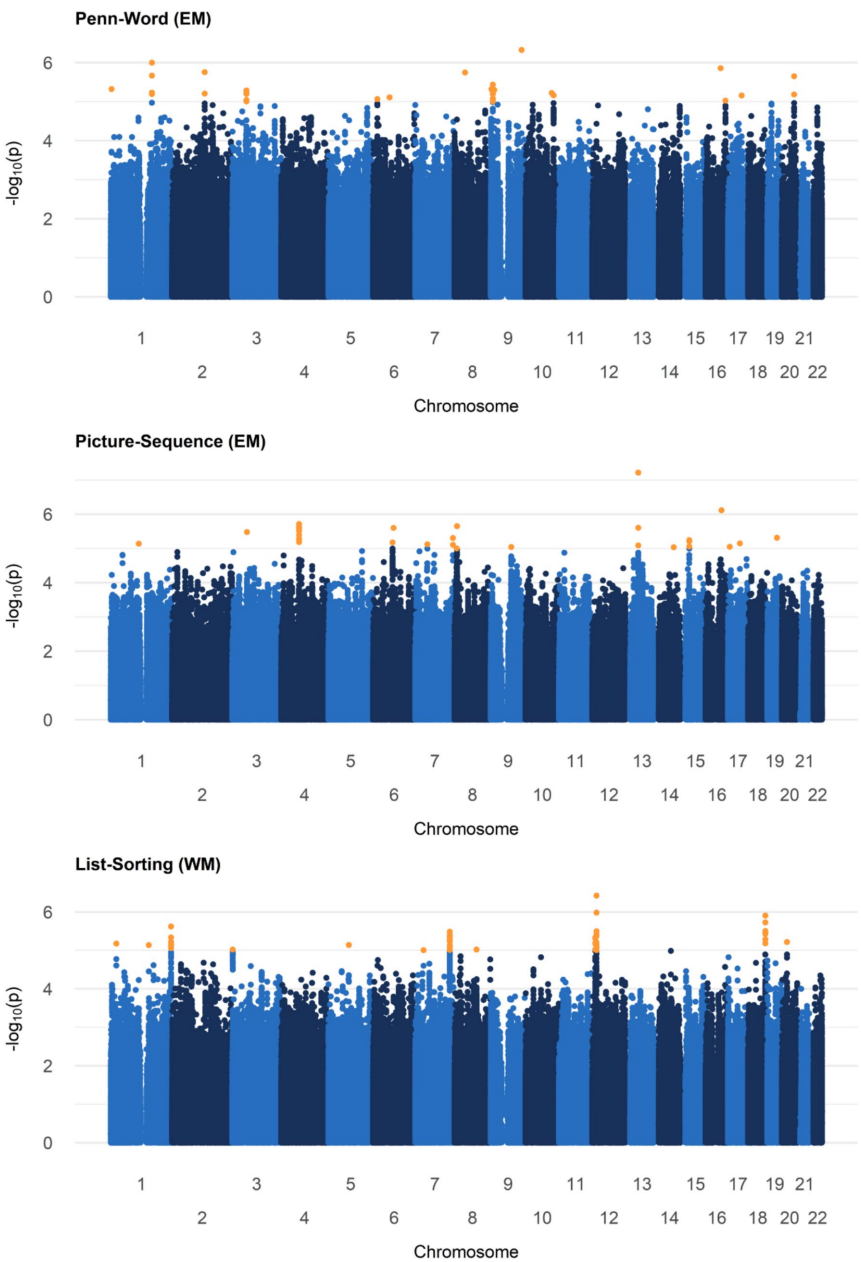
GWAS分析中,没有变异达到传统基因组显著性水平(p<5×10-8),但在宽松阈值下,Penn-Word测试发现17个SNP,Picture Sequence测试发现16个SNP,List Sorting测试发现11个SNP。λ值接近1(1.04-1.13),表明不存在明显的p值膨胀,结果可靠。
有趣的是,虽然top SNP在不同测试间没有重叠,但全基因组水平的遗传相关性分析显示,Picture Sequence与Penn-Word测试之间遗传相关性最高(rG=0.59),Picture Sequence与List Sorting次之(rG=0.56),Penn-Word与List Sorting最低(rG=0.35)。这表明不同记忆类型共享部分遗传基础,但共享程度存在差异。
通过连锁不平衡扩展和功能注释,研究将SNP映射到候选基因:Penn-Word测试对应25个基因,Picture Sequence测试对应35个基因,List Sorting测试对应10个基因。值得注意的是,SERPINE3基因在Picture Sequence分析中接近MAGMA基因组显著性水平(p=1.31×10-6),该基因与阿尔茨海默病和朊病毒疾病相关。
尽管基因列表在不同记忆测试间没有重叠,但eQTL分析显示这些基因在大脑组织中均有表达,支持它们与神经功能的生物学关联。
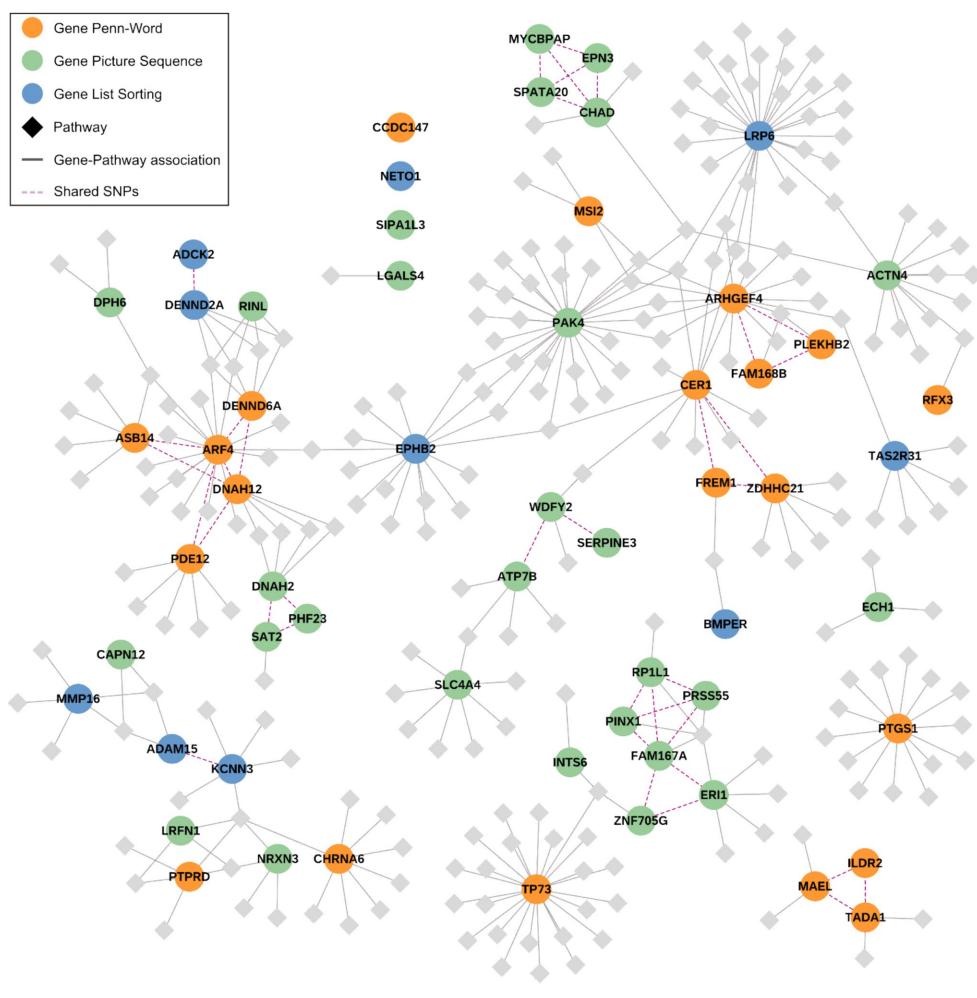
通路分析揭示了更深层次的生物学一致性。三个记忆测试共识别229个独特通路关联,其中38个通路连接两个及以上基因,34个通路在不同记忆测试间共享基因。经过合并冗余通路(基因重叠≥80%)后,25个核心通路节点浮现出来。
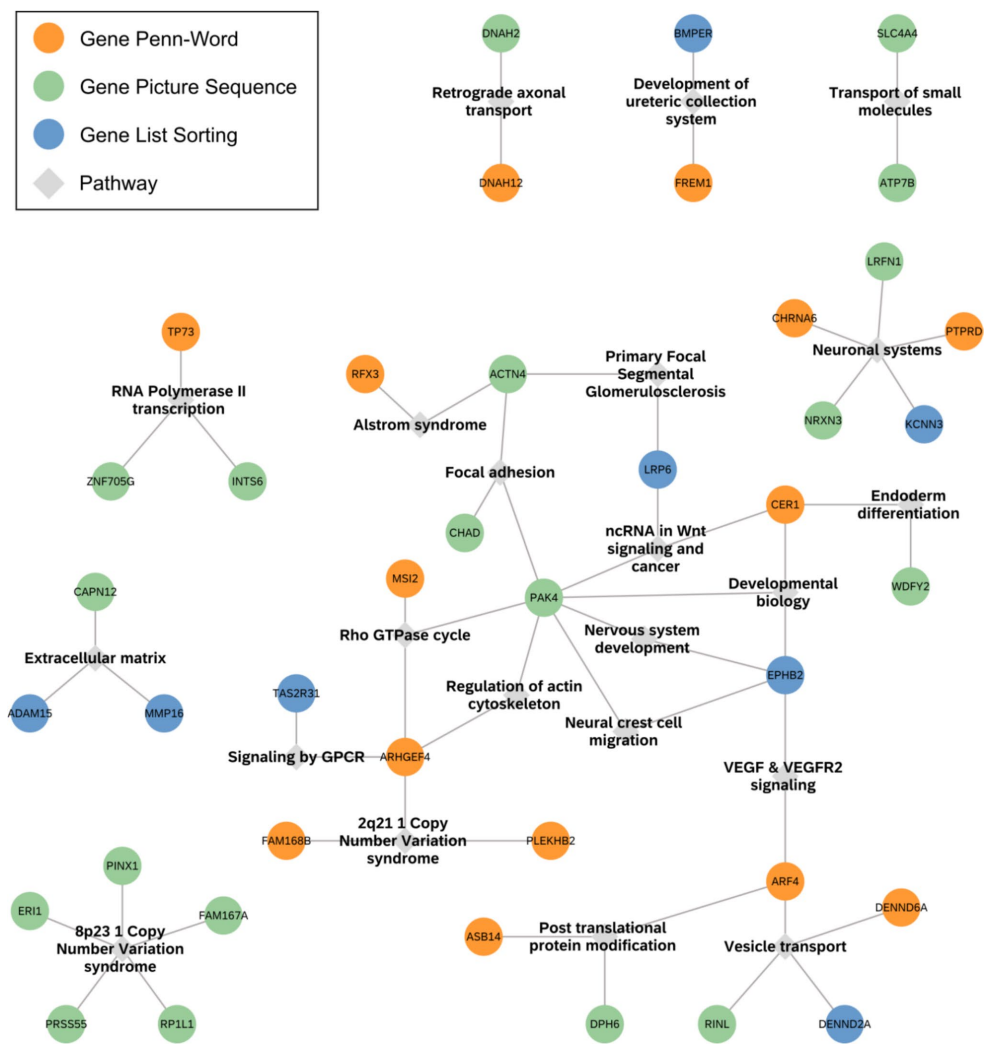
最重要的发现是"神经元系统"通路节点,它包含突触小泡运输、膜运输和突触蛋白-蛋白相互作用等过程,成为连接不同记忆测试基因的关键枢纽。其他重要通路包括EPHRIN神经发育通路、G蛋白偶联受体信号、WNT信号、钙离子依赖性信号传导等。
结构变异分析发现,8p23.1和2q21.1拷贝数变异区域与记忆表现相关。8p23.1倒位先前与神经质、抑郁等表型相关,而2q21.1区域缺失与发育迟缓、注意力缺陷多动障碍和癫痫有关。
与GWAS Catalog中四个记忆研究的对比显示,在基因水平重叠有限,但在通路水平存在显著一致性,重叠率最高达68%(Picture Sequence与Hatoum等人的数字广度测试)。这种差异进一步支持通路分析在发现生物学信号方面的优势。
研究结论强调,记忆的遗传架构具有高度多基因性和复杂性,传统GWAS方法在样本量有限的深度表型研究中容易错过重要生物学信号。通过宽松p值阈值结合系统生物学分析,能够发现单基因水平无法检测的共享机制。
这种通路水平的收敛性提示,尽管不同记忆类型可能受到不同基因集的影响,但它们共享关键的分子机制,如突触可塑性、神经发育和免疫调节等过程。这些发现不仅为理解正常记忆的生物学基础提供新视角,也为记忆相关疾病(如阿尔茨海默病、精神分裂症、抑郁症)的研究开辟了新途径。
该研究提出的分析流程已作为开源工具共享,适用于其他复杂多基因性状的研究。未来在更大规模、更多样化人群中的验证,以及结合多组学数据的整合分析,将进一步深化我们对记忆遗传机制的理解。
 生物通微信公众号
生物通微信公众号
知名企业招聘