��Marine Biotechnology����Production of Biopharmaceutical Proteins from Scallop Hemocytes as a Bioreactor Using Improved Transfection Conditions
�༭�Ƽ���
�������о�ּ��Ӧ�Դ�ͳ���鶯��ϸ����˾�(E. coli)������ҩ����ƽ̨�ڵ����ʷ��������ȱ���벡����Ⱦ���յȷ���ľ��ޡ��о���Ա������һ������Ϻ���ȱ�(Mizuhopecten yessoensis)ԭ��Ѫϸ����������Ϊ���ﷴӦ��������ƽ̨��ͨ���Ż�תȾ�������ɹ�ʵ������������������(hGH)�ı����֤ʵ�������˴ٺ�ϸ��������(hEPO)�ķ��ڡ������о��״�֤����������������嶯��ϸ���еı��Ϊ����������ҩ���������һ�־���DZ������ƽ̨��
����
������ҽҩ����������ҩ�����������ҩ�����ȵ��ء��������غ���壬�ѳ�Ϊ���ƶ��ּ����Ĺؼ���Ŀǰ����Щҩ����Ҫ�������鶯��ϸ������CHOϸ������ϸ������˾�E. coli����������Ȼ������������������������������ޣ����鶯��ϸ�����ܽ��и��ӵ������������ʼӹ��������ڲ�����Ⱦ�ķ��գ���ϸ��ϵͳ����������൰���ʱ���ķ�������Σ����ǻ����������Ӱ��ҩ��Ĺ������ȶ��ԡ���ˣ���ѧ����һֱ��Ѱ�Ҹ���ȫ������Ч���������ƽ̨��
���ڣ�һ����ڡ�Marine Biotechnology���ϵ��о�����Ŀ��Ͷ���˺���������ԣ��Dz����ϳ�����Ϻ���ȱ�(Mizuhopecten yessoensis)���о���Ա�����Ե���������������ȱ���Ѫϸ����Ϊ�͡����ﷴӦ�������������൰����ҩ���������������Щ����˼�飬���ȱ�Ѫϸ��ӵ����������ƣ��������ڴ�ѪҺ�д������ྻ�ػ�ȡ���������¶Ƚϵͣ�10�C20��C���������������Ƴ���ϸ���Ͳ�������ֳ������Ҫ���ǣ���ǰ�о����֣�һ��Դ��˫���ಡ����Ⱦ����(Ostreid herpesvirus-1�� OsHV-1)�������ӣ�����˫����ϸ����������ǿ�Ļ��������ԣ���Ϊ�����ȱ�ϸ��������Դ�����ṩ�˿��ܡ�
Ϊ����֤��һ���룬�о��Ŷ�������ҪΪ�ȱ�Ѫϸ���������¹�����������Ч��������ˮ�ߡ�����ϵͳ���Ż�����12�װ��е�ϸ��������תȾ�������漰�ĸ��ؼ���������ù��-��ù��(PS)Ũ�ȡ�����ϸ��������Ѫ�ܰ����������ı����Լ�תȾ�Լ���������ȷ������������Ϊ��PSŨ��20 U/mL������2 �� 106��ϸ��/�ף���600 ��Lϡ��Ѫ�ܰ���300 ��L˫��Ũ��L-15(L15��2)��������ϣ�����900 ��L��ϸ�����������м���200 ��L X-tremeGENEתȾ�����
�����뷽���ؼ��������
�о�ʹ���������ձ�½������ֳ���ij���Ϻ���ȱ����ɼ���Ѫ�ܰͻ�ȡԭ��Ѫϸ����������������ʵ�鼼���������������в�ͬ��ǩ��EGFP��V5/His��HiBiT��������������(hGH)���˴ٺ�ϸ��������(hEPO)�������壻ʹ�û�ѧתȾ�Լ������嵼���Ż���������ȱ�Ѫϸ����ͨ��ӫ����������PCR(RT-qPCR)������������ӡ��(Western blot)��ø�����������ⶨ(ELISA)�ȶ��μ������Ŀ�군�ı��������������HiBiT���ϵͳ����hEPO�ķ���Ч�ʣ���ͨ����-N-����øF(PNGase F)�������������ʵ�N-�����ǻ���ģʽ��
����
1. ��������ȱ�Ѫϸ�������ʲ�����������תȾ����
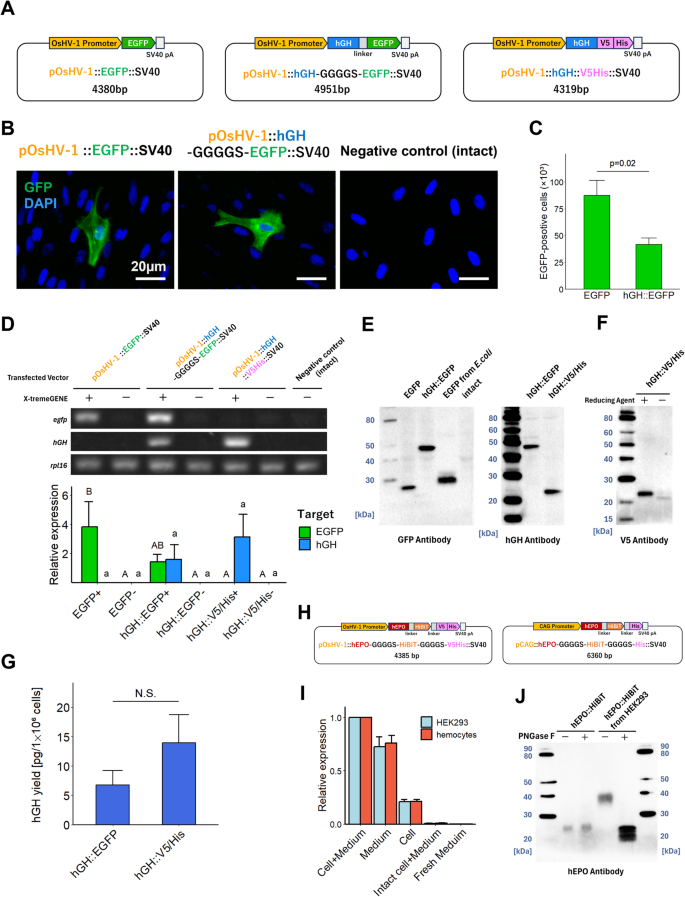
�о���Աͨ������ǿ����ɫӫ�⵰��(EGFP)Ϊ������������˲�ͬ������תȾ��EGFP����ϸ�����������Ӷ�ȷ����ǰ������������ϡ�����������������תȾЧ�ʣ�Ϊ�����������鵰�춨�˻�����
2. �ȱ�Ѫϸ����hGH�ļ���붨��
�����������£��о���Աʹ��������Я����ͬ��ǩ��EGFP��V5/His����hGH�������塣ӫ�����ֱ�ӹ۲쵽��Ѫϸ����hGH::EGFP�ںϵ��ı��RT-qPCR��mRNAˮƽȷ����hGH�ı�����ұ��������������С�����ԣ���С��hGH::V5/His������ߣ���Western blot�ڵ�����ˮƽ�ֱ��ÿ�EGFP�Ϳ�hGH�������Ԥ�ڴ�С���������ر�أ��ڷǻ�ԭ�����½��е�Western blot��ʾhGH::V5/His������������Ǩ�ƣ��������ȱ�Ѫϸ���б����hGH�γ��˷����ڶ��������������ȷ�۵��;���������ԵĹؼ���־�����ͨ��ELISA���������hGH::V5/His�IJ�����ߣ��ﵽ13.92 �� 4.77 pg/1 �� 10
6��ϸ����
3. ȷ���ȱ�Ѫϸ����hEPO�����������ǻ���ģʽ
Ϊ�������ȱ�Ѫϸ�����������ӵ����ʵ��������о���Ա�����˴���HiBiT��ǩ��hEPO��HiBiT�����ʾ���ȱ�Ѫϸ���ܹ���Լ�ķ�֮�������hEPO::HiBiT�����ڵ��������У������Ч��������HEK293ϸ��ϵ�൱��Ȼ����Western blot�������PNGase F������������Ѫϸ�����ڵ�hEPO::HiBiT����δ��N-�����ǻ�����������HEK293ϸ���б���ġ������ǻ������ε�hEPO��ͬ��
����������
�����о��״γɹ��Ż���Ϻ���ȱ�ԭ��Ѫϸ��������תȾ���������ڴ˻����ϣ��״��ڷ���(mRNA)�͵�����ˮƽ��֤ʵ���������hGH��hEPO���������嶯��ϸ���гɹ�������У������hGH��֤ʵ�γ�����ȷ�ķ����ڶ��������hEPO��չʾ�˸�Ч�ķ������������־���ȱ�Ѫϸ����Ϊһ��Դ�Կ�ʳ�ú�����������������ﷴӦ��ƽ̨�������֤��
��ƽ̨�߱�����DZ�����ƣ�Ѫϸ�����ڻ�ȡ�������¶ȵͿ��ܽ�����Ⱦ���ա��Լ�����ǿ���OsHV-1������ʵ�ָ�Ч���Ȼ�����о�Ҳָ���˵�ǰ�ľ����ԣ����ȣ�����ĵ����ʲ����Ե��������ѽ�����ƽ̨�������ࡢ����ϸ���ȣ����������ԭ��ϸ�������תȾЧ�ʲ�����йأ���Σ������hEPOȱ��N-�����ǻ�������ʾ�ȱ�ϸ�����ǻ������ƿ����벸�鶯�ﲻͬ�������Ӱ��ijЩ��Ҫ�ض��ǻ���ģʽ���ܷ��ӹ��ܵ������Ե����ʵĻ��ԡ���ˣ�δ����Ҫ�Ա���ĵ����ʽ������������֤��������̽�����嶯��ϸ���ĵ���������������
������ˣ������о�Ϊ������ҩ����������һ��ȫ�µ�·���������ȱ�ϸ��ϵ���������ķ�չ����������ο��ȱ��н�����ϸ��ϵ���Լ����ȱ���Ѫ��ϸ����ʶ�����룬δ���������ԭ��ϸ���ı��������⣬�Ӷ��ƶ���һ����ϸ��ƽ̨����ʵ��Ӧ�ã�Ϊ�ɳ����Ͱ�ȫ��������ҩ�����ṩ�µ�ѡ��



 ����ͨ�Ź��ں�
����ͨ�Ź��ں�