
-

����ͨ��
����ץס�����Ƽ�
����������
�ܵ���/Ф�����Ŷӿ���������Τ-����鰷ż�������˫�е�Эͬ�������·�ʽ
�����壺 �� �� С �� ʱ�䣺2026��03��01�� ��Դ��������ѧҩѧԺ
�༭�Ƽ���
���� 2026��2��26�գ� �� Ժ ��Ȼҩ�P����ҩ��ȫ���ص�ʵ���� �ܵ��� /Ф���� �о��Ŷ��� Journal of Medicinal Chemistry ���߷�����Ϊ��Zanamivir-Amantadine Conjugate: A Dual-Action Agent with Broad-Spectrum Synergistic Antiviral Efficacy�����о�����
���в�����Ϊ�߶ȴ�Ⱦ�Եĺ�������ԭ�壬ƾ����������ٵĻ���ͻ�������������������������п�����ҩ��ķ���Ч������ǰ�ٴ�һ������ø��NA�����Ƽ������˾��Τ��������Τ������ȫ��Χ�ڳ��ֲ�ͬ�̶ȵ���ҩ���⡣���ͻ�ơ����е㡢����ҩ����Ч˥�����Ĵ�ͳ·������������������ҩ������Эͬ���Ƶ����Ϳ����в��ԣ���Ϊ������ҩ���з�����Ҫǰ�ؿ��⡣

2026��2��26�գ���Ժ��Ȼҩ�P����ҩ��ȫ���ص�ʵ�����ܵ���/Ф�����о��Ŷ���Journal of Medicinal Chemistry���߷�����Ϊ��Zanamivir-Amantadine Conjugate: A Dual-Action Agent with Broad-Spectrum Synergistic Antiviral Efficacy�����о����ġ����о��ԡ�Эͬ˫�е��Ԥ��Ϊ�������ͨ�����Ӳ���ľ���ƣ���NA���Ƽ�������Τ��M2����ͨ����ϼ�����鰷����ѧ������ż�������һ����˫�ػ��Ƶ�ȫ�¿����з��ӣ�Ϊ������ҩ��ӡ���һ�е����ơ���Эͬ˫�е����ء�ת���ṩ���������������
����������ϵ�з����У���ѡ������7jչ�ֳ���ǿ���ۺ����ܡ��û����ﲻ������������������Τ��NA�ĸ�Ч���ƻ��ԣ���ͨ���������鰷����ˮ��ǩ��ʵ������NA�����յ����⣬���������ӡ�����+���⡱��˫�ش��������ͬʱ��ż����������������������Τ��Ĥͨ�ԣ���������ΤƬ���ֿɲ���������鰷�յ���ϸ���������ɷ�Ӧ���ڷ����ڲ�ʵ��������Ч�������ľ�ϸƽ�⡣
���⿹����ʵ�������7j����NA��M2��ҩͻ�������ڵĶ��ּ������в�����H1N1��H3N2�������ֳ�������ǿЧ�����ƻ��ԣ�EC50����11.13 nM���ϰ�˾��Τ��������Τ����Լ2������ϸ�������������ڽ���鰷�������о���һ��֤ʵ��7j��ͨ������鰷��ˮ��ǩ�鵼NA�������بC����ø��;��ѡ���Խ��⣨DC50 = 636.6 nM�����ڹ�������֮�����������ˮƽ���ЧӦ��ͬʱ��7j����Ч���M2����ͨ�����ܣ����Խ���鰷��ҩͻ���壨S31N/I32N��S31N/G34E��S31N/R45H�����ֻ��ԣ����������˶���ҩ������Ӧ��������
ҩ������ѧ�о���ʾ��7j����ע���İ�˥�ڴ�5.72Сʱ����������Τ�ӳ�Լ14��������ͨ����������ǻ����θ�ȶ���;����ҩ�����ֳ����õĿ���DZ�����ڼ���H1N1�����Ը�ȾС��ģ���У����ξ�����ҩ7j����ʵ��100%��������Ч��������������Τ����˾��Τ��������Τ����Ԥ���Ը�ҩģʽ��ͬ��չ�ֳ��������ơ�����֯����ѧ�����һ��֤ʵ��7j���������ⲡ���յ��ķ���֯���ˣ���δ�۲쵽���ԸΡ�����������źš�
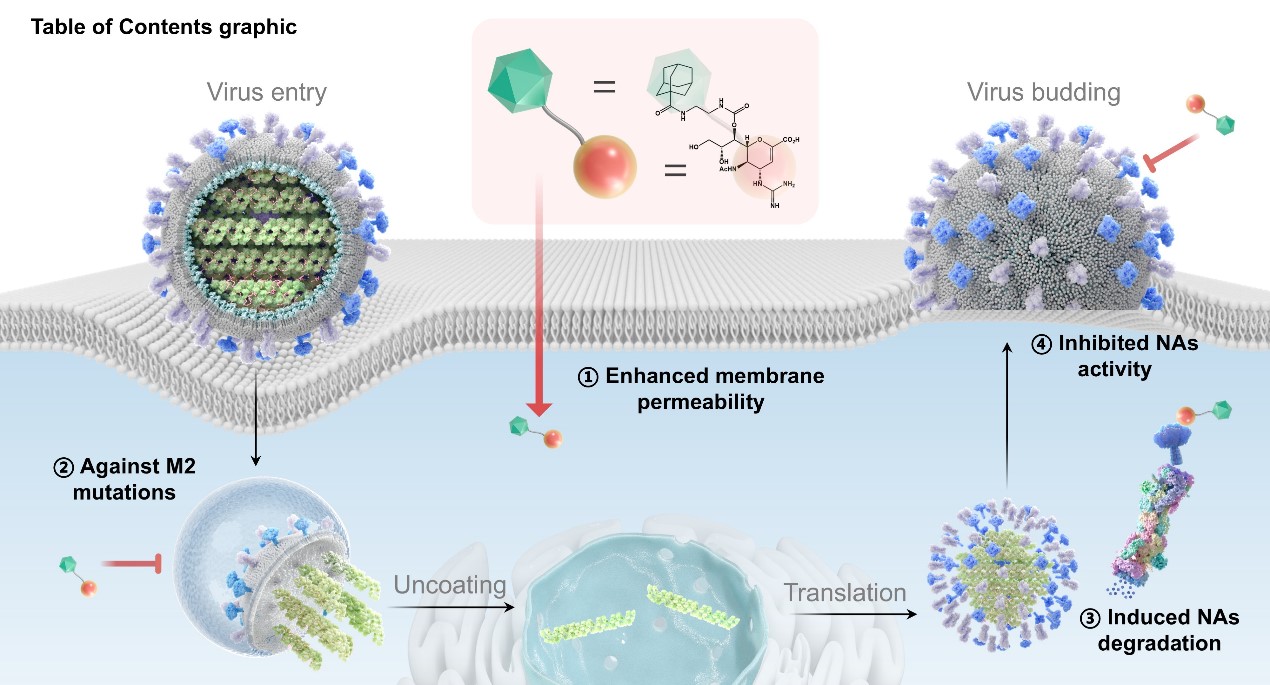
���о����������һ�ֿ���֤�ġ�˫�е�Эͬ+�е����⡱��������ģʽ��ҲΪ������ҩ�ṹ�Ĺ�����������������ṩ�˷�����ͨ������ż��ʵ��ҩЧЭͬ����ҩͻ���밲ȫ���Ż���ͳһ��Ϊ������ҩ���з��������µIJ��ԣ���Ӧ��δ�����ܳ��ֵ���ҩ���ж��������Ҫ��ʾ���塣
���о���ù�����Ȼ��ѧ���𡢹����ش�Ƽ�ר��ƻ�������ʡ�Ƽ������������о���Ժ�Ƽ�ר�����Ŀ֧�֡���ʿ�����������������Ͷκ��Ϊ���Ĺ�ͬ��һ���ߣ��ܵ���������Ф�����о�ԱΪͨѶ���ߡ�������ѧҩѧԺ��Ȼҩ�P����ҩ��ȫ���ص�ʵ����Ϊ��һ��ɵ�λ��
�������ӣ�https://pubs.acs.org/doi/full/10.1021/acs.jmedchem.5c03547
��Ȼҩ�P����ҩ��ȫ���ص�ʵ����