编辑推荐:
本综述系统阐述了成纤维细胞生长因子(FGF)家族的复杂世界。文章深入剖析了FGF/FGFR信号通路的分子机制、调控网络及其在胚胎发育、组织稳态维持、代谢调节和癌症等疾病中的双重角色,并特别强调了靶向该轴在组织再生(激动剂策略)与癌症治疗(拮抗剂策略)中的巨大转化潜力,为理解这一关键信号系统提供了全面、前沿的整合视角。
结构与分类:一个多样的信号家族
成纤维细胞生长因子(FGF)家族包含22个结构相似的成员,它们在进化上高度保守,共同构成了一个调控胚胎发育、组织再生和全身代谢稳态的关键信号系统。根据其作用模式,FGF家族可分为三大功能类别:旁分泌型(经典)FGF、内分泌型FGF和胞内型FGF。大多数FGF成员(如FGF1-FGF10, FGF16-FGF18, FGF20, FGF22)属于旁分泌型,它们作为局部信号分子,通过与细胞表面的FGF受体(FGFR)结合发挥功能。内分泌型FGF(FGF19, FGF21, FGF23)则通过血液循环远距离作用于靶器官,像激素一样调节胆汁酸、葡萄糖和磷酸盐代谢。胞内型FGF(FGF11-FGF14)不分泌到胞外,主要在细胞内发挥调节电压门控钠通道等功能。
FGFR是介导FGF信号传递的酪氨酸激酶受体,包括FGFR1-4四个成员,并通过组织特异性选择性剪接产生不同的亚型(如FGFR1b/c)。FGF与FGFR的特异性结合需要辅助因子的参与:旁分泌FGF依赖硫酸乙酰肝素蛋白聚糖(HSPG),而内分泌FGF则需要Klotho蛋白(α-Klotho或β-Klotho)作为共受体,形成FGF-FGFR-Klotho三元复合物,以启动下游信号。
信号通路:从经典到非经典的调控网络
FGF/FGFR信号传导主要通过经典的激酶依赖通路进行。当FGF与FGFR结合后,受体发生二聚化并自磷酸化,进而招募并激活下游的停泊蛋白FRS2α和磷脂酶Cγ(PLCγ)。FRS2α的磷酸化位点招募接头蛋白GRB2,进而激活两条主要下游通路:1)通过SOS激活RAS/RAF/MEK/丝裂原活化蛋白激酶(MAPK)级联反应,包括ERK1/2、p38和JNK MAPK,调控细胞增殖、存活、分化和迁移;2)通过GAB1激活磷脂酰肌醇-3-激酶/蛋白激酶B(PI3K/AKT)通路,促进细胞存活并抑制凋亡。另一方面,活化的PLCγ水解磷脂酰肌醇-4,5-二磷酸(PIP
2)生成三磷酸肌醇(IP
3)和二酰基甘油(DAG),分别诱导细胞内钙离子释放和蛋白激酶C(PKC)激活,参与细胞迁移等过程。
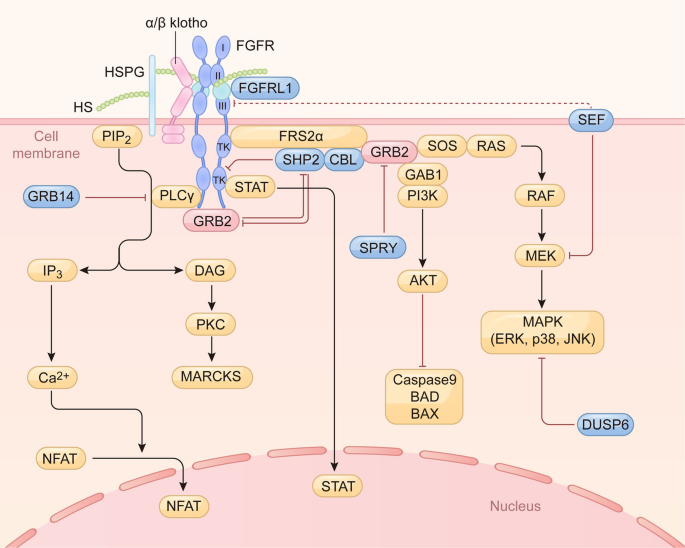
除了经典通路,FGF信号还存在不依赖FGFR激酶活性的非经典方式。例如,FGF2可直接与整合素αvβ3结合,或通过跨膜蛋白聚糖(如多配体蛋白聚糖-4)传递信号,影响血管生成和细胞迁移。神经细胞粘附分子(NCAM)和N-钙粘蛋白也能在无FGF配体的情况下直接与FGFR相互作用,触发下游信号,参与神经发育和肿瘤转移等过程。
FGF信号受到精密的多层次调控。一系列负反馈机制确保信号的精确性和瞬时性,包括:1)Sprouty(SPRY)蛋白通过干扰GRB2或RAF抑制RAS/MAPK通路;2)SEF蛋白通过结合MEK-ERK复合物阻止ERK入核;3)双特异性磷酸酶6(DUSP6/MKP3)直接去磷酸化ERK使其失活;4)E3泛素连接酶CBL介导FGFR和FRS2α的泛素化降解,从而终止信号。
生理功能:发育与稳态的指挥官
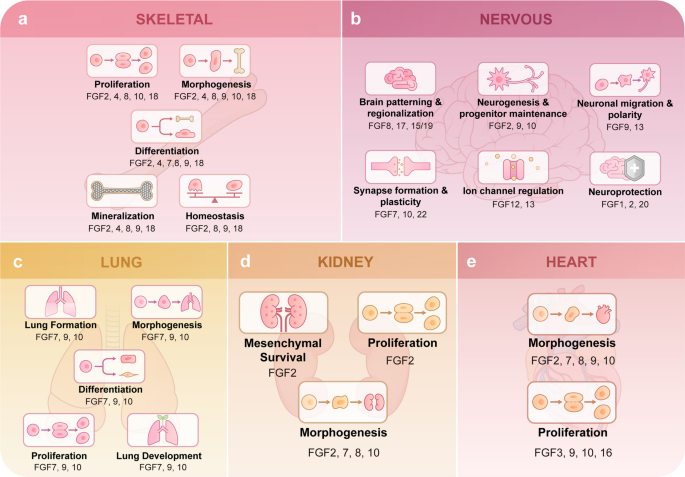
FGF信号在多种器官的发育和成年期组织稳态维持中扮演着“指挥官”的角色。在骨骼系统中,FGF2、FGF4、FGF8、FGF9、FGF10、FGF18等成员协同调控骨骼细胞的增殖、分化和矿化,对肢体形态发生和骨骼生长至关重要。在大脑中,FGF8、FGF17和FGF15/19参与脑部图式形成和区域化,而FGF2、FGF9、FGF10等则维持神经发生和突触可塑性。在肺部,FGF7、FGF9和FGF10是肺发育的主调控因子,共同协调肺组织的形态发生、上皮分支和细胞分化。在心脏,多个FGF成员调节心脏形态发生和心肌细胞增殖。在肾脏,FGF2、FGF7、FGF8、FGF10等介导肾脏的形态发生。
内分泌FGF(FGF19/21/23)作为系统性代谢调节因子,在维持能量和矿物质平衡中发挥核心作用。FGF19由回肠响应进食而分泌,作用于肝脏,负反馈抑制胆汁酸合成。FGF21主要由肝脏产生,响应营养和代谢压力,促进葡萄糖摄取和脂肪酸氧化,改善胰岛素敏感性和能量消耗。FGF23则由骨细胞分泌,作用于肾脏,促进尿磷排泄并抑制活性维生素D的合成,是磷酸盐稳态的关键激素。
疾病关联与治疗前景:一把双刃剑
FGF/FGFR信号的异常与多种疾病密切相关,这使其成为极具吸引力的治疗靶点,但其治疗策略呈现出“双刃剑”的特性。
在代谢性疾病领域,激活FGF信号通路显示出巨大潜力。工程化的FGF1、FGF19类似物(如Aldafermin/NGM282)和FGF21类似物正在被开发用于治疗非酒精性脂肪性肝炎(NASH)、2型糖尿病和肥胖症。它们通过改善胰岛素敏感性、减少肝脂肪变性和炎症、调节能量代谢等机制发挥作用。
然而,在癌症中,FGF/FGFR信号通路常常被异常激活,成为驱动肿瘤发生、进展、血管生成、耐药和免疫逃逸的“引擎”。FGFR基因的扩增、突变或融合在多种癌症中频发。因此,抑制该通路成为抗癌策略的核心。目前,多种小分子FGFR酪氨酸激酶抑制剂(如Erdafitinib、Pemigatinib、Infigratinib)和针对特定FGFR亚型的单克隆抗体已获批或处于临床试验阶段,用于治疗伴有FGFR异常的尿路上皮癌、胆管癌等恶性肿瘤。
此外,FGF信号在组织修复和再生医学中也前景广阔。局部递送FGF2能促进骨折愈合和骨缺损修复。FGF7(角化细胞生长因子)可用于治疗黏膜损伤。基于FGF的信号调控策略在神经再生、血管生成和伤口愈合等领域均有探索。
总之,FGF家族是一个功能复杂且调控精细的核心信号系统,深度参与生命过程的方方面面。对其分子机制和生理病理角色的深入理解,不仅揭示了发育与疾病的基本规律,更开启了针对代谢性疾病、癌症和组织修复的精准治疗新纪元。未来,通过工程化改造配体、开发特异性更高的受体调节剂以及探索联合治疗策略,FGF靶向疗法有望为人类健康带来更多突破。




 生物通微信公众号
生物通微信公众号