
-

����ͨ��
����ץס�����Ƽ�
����������
Cell Reports | ������ѧѧԺ�ְ����Ŷӿ�������CRISPR�����������༭���ߣ�ʵ��������mtDNAͻ��ĸ�Ч����
�����壺 �� �� С �� ʱ�䣺2026��03��21�� ��Դ���㽭��ѧ������ѧѧԺ
�༭�Ƽ���
����ϸ����Ĥϵͳ����Ĥ���ҹ�������ϸ���ṹ��Ϊ������ӵ�����ֲ���������Ӧ�ṩ�˸߶Ⱦ��ܵ�����������ϸ���ṹ��ּ�����Ԫ���������ھ�����Ϊ����ϸ����л�Ķ�̬���������ṩȫ���ӽǣ�����Ϊ���ཡ����Ԥ�뼲�������ṩ��˼·�����������о�������RNA��Ϊϸ�����������Ҫ����Ԫ�����߶Ȳ�����Ĥ����ϵͳ����ϸ����ϸ�ṹ����ɹ�������ع��ܡ��㽭��ѧ������ѧѧԺ�ְ����Ŷ����RNA�Ŀռ�ֲ����ɣ�����RNA���һ���...
ϸ����Ĥϵͳ����Ĥ���ҹ�������ϸ���ṹ��Ϊ������ӵ�����ֲ���������Ӧ�ṩ�˸߶Ⱦ��ܵ�����������ϸ���ṹ��ּ�����Ԫ���������ھ�����Ϊ����ϸ����л�Ķ�̬���������ṩȫ���ӽǣ�����Ϊ���ཡ����Ԥ�뼲�������ṩ��˼·�����������о�������RNA��Ϊϸ�����������Ҫ����Ԫ�����߶Ȳ�����Ĥ����ϵͳ����ϸ����ϸ�ṹ����ɹ�������ع��ܡ��㽭��ѧ������ѧѧԺ�ְ����Ŷ����RNA�Ŀռ�ֲ����ɣ�����RNA���һ�����RNA compartmentalization�����䱳��Ĺ��ܵ����о����Ŷ�ǰ�ڿ�����ϸ���������ʹ�����ϵ�����Ƴ�������ϸ���������DZ���RNA��lncRNA��ͼ�ף��ڴ˻����ϣ������ʾ��������lncRNA GAS5��������ѭ����л���ҽ����еĵ��ػ��ƣ�Nature Metabolism��2021�����Լ�lncRNA SNHG6�鵼ϸ�����Ӵ����γɲ����ص��̴���л����Ҫ���ܣ�Nature Metabolism��2022������������Ϊ������ȻRNA����ϸ������ת�˻��Ƶ춨�����ۻ�����
���ڶ���ϸ���ṹ�У���������Ϊϸ���ġ������������ͺ��Ĵ�л��Ŧ��ӵ�����������Ļ����飨mtDNA���ͷ���ϵͳ����������������ת¼�뷭�����ά���������ữ��ATP���ɲ��ɻ�ȱ��һ��mtDNA����ͻ�䣬�������������Լ������ļ����������Ŵ��Լ�����ȫ����Լ1/5000����Ŀǰ�����mtDNA�Ļ���༭������Ҫ����пָ����ø��ZFNs����ת¼����������ЧӦ�����ø��TALENs���ȣ���Щ�������༭���߲�������RNA��������������Ƹ��ӡ���������Բ�������⡣CRISPR-Cas9ϵͳ�ں˻�����༭��չ�ֳ���Ч����ݵ��ص㣬�����������ܵ�˫��Ĥ�ṹ����sgRNA���Խ�����������ʣ�������Cas9������������ı༭Ч�ʼ��ͣ���0.03%-0.23%����������������CRISPRϵͳ�������弲�������е�DZ������ˣ����ͨ�����ӹ����ֶζ������sgRNA���������Ч��������˫��Ĥ��ʵ�־���λ������������Ϊ���CRISPRϵͳӦ�������������༭����Ҫͻ�ƿڣ�Ҳ��Ϊ�������Ŵ����������ṩDZ�ڵײ㹤�ߡ�
���գ��㽭��ѧ������ѧѧԺ�ְ��������Ŷ���Cell Reports��־���߷�����ΪA CRISPR-based mitochondrial gene therapy tool derived by engineering guide RNAs ���о����ġ����о�ͨ�����������嶨λlncRNA��ת�˻��ƣ�������һ������RNA������������У�RMTS�����������˸�Ч�������RMTS-CRISPR���������༭ϵͳ��ΪmtDNAͻ����ؼ����������ṩ��ȫ�²��ԡ�

�о��Ŷ���������ϸ���������ʹ�����ϸ�ͨ���������������������帻��lncRNAͼ�ף����м�����199��������λ���������lncRNA��ͨ��ϵͳ���������빦����֤��ɸѡ��17�����б��������嶨λ�����ĺ�ѡ���ӣ�����lncRNA RP11-46H11.3���ֳ���ǿ�������嶨λ��������һ�������о�������RP11-46H11.3ͨ�������RNAʶ�����RRMs�������������RNA��ϵ��ף�RBPs��IGF2BP2��ELAVL1�����Խ�ϣ��Ӷ��鵼����������İ���ת�ˡ��ù���������RNA���������ṹ��������л����Эͬ�������ṹ��Ϊ���Ǽܡ���¶���λ�㣬�����Ļ����ṩ������ʶ�𡣻����������ƣ��о��ŶӴ�RP11-46H11.3�����ռ�����һ��30���������ST2���У�����ΪST2-RMTS����������ߵ�RNA�������������Ч�ʡ�
Ϊ���sgRNA���������ƿ�����о��Ŷӽ�ST2-RMTS��sgRNA�ںϣ�����������嶨λ�ź��ģ�MTS�����ε�Cas9��MTS-Cas9����������RMTS-CRISPR�༭ϵͳ���������ø����ʵ�������RMTS���ںϲ�Ӱ��sgRNA�Ļ��Լ�Cas9���и�Ч�ʡ���HEK293Tϸ���У�RMTS-CRISPR�ɸ�Ч�����и�MT-ND1��MT-ND2��MT-ND4�ȶ�������������һ����Ϊѡ�������ͻ��mtDNA�ṩ������ļ����������о��Ŷӽ���ϵͳӦ�����ٴ�������m.3243A>G������ͻ��ϸ��ģ���У������ʾRMTS-CRISPR��Ԥʹ����������DNA������������26.37%����Чʵ����ͻ���������������ͻ��mtDNA���ɣ����ָ�ϸ����ATP�����������뾭���Mito-TALENs������ȣ�RMTS-CRISPR�༭Ч���൱��������Ƹ�Ϊ��ݡ�������չҲ����
�����弲�����ٴ�����ͨ����ͻ��mtDNA����������ֵ��ء����о�����RMTS-CRISPRʵ����Լ26%��ͻ�为�ɽ��ͣ�Ϊ��ϵͳ��DZ���ٴ�Ӧ���ṩ�˳������ݡ�����ͻ�为�ɴ���60%�C80%���ٽ综�ߣ�����ͻ�为��������������ֵ���£��Ӷ����ƻ��ӻ�������չ�����⣬������֢���ߣ�Ҳ�ܲ��ָֻ���������������ܣ�����������лȱ�ݡ��о��Ŷӱ�ʾ��δ������һ���Ż�RMTS���нṹ��RMTS-sgRNA�ȶ��ԣ�����ϵ�����ϵ�������������Ч�ʣ��ƶ��ü������ٴ�ת�������о�����Ϊ��������������ṩ�������ߣ�ҲΪ��������RNA��������ת�˻����ṩ����Ҫ���⡣
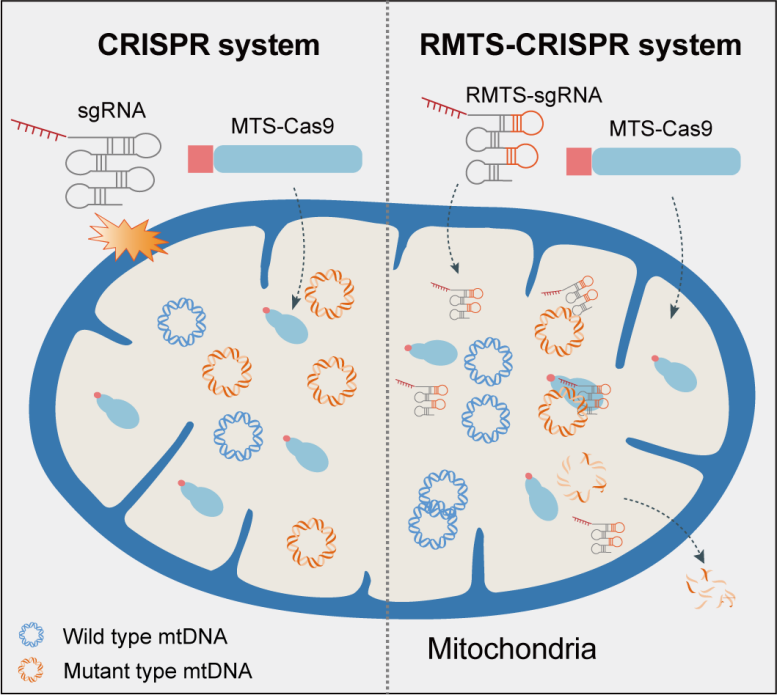
ͼ1 RMTS CRISPRϵͳ�������ͻ��mtDNAʾ��ͼ
�㽭��ѧ������ѧѧԺ��ӱ��������ͳ��Ϊ���Ĺ�ͬ��һ���ߣ��ְ�������ΰǿ������ΪͨѶ���ߡ��о��õ��˹�����Ȼ��ѧ����RNA�ش��о��ƻ��ص���Ŀ�����ҽܳ������ѧ���𡢿Ƽ�����2030�ش�ר������ص��з��ƻ����㽭ʡ�����㡱�з����ؼƻ�����Ŀ��������
ԭ�����ӣ�https://www.sciencedirect.com/science/article/pii/S2211124726000367