
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Cell Death & Differentiation|王陈继/叶定伟/常坤团队揭示DPP9酶活抑制剂介导抗肿瘤免疫的新机制
【字体: 大 中 小 】 时间:2026年03月22日 来源:复旦大学生命科学学院
编辑推荐:
3 月 14 日,复旦大学生命科学学院王陈继团队和附属肿瘤医院叶定伟 / 常坤团队在 Cell Death & Differentiation 发表题为 DPP9 inhibition boosts antitumor immunity by disrupting BRISC-mediated PD-L1 expression in clear cell renal cell carcinoma 的研究论文
免疫检查点治疗已成为透明细胞肾细胞癌系统治疗的重要组成部分,但临床上仍普遍面临应答率有限、免疫逃逸和耐药等问题。作为肿瘤免疫抑制网络中的核心分子,PD-L1虽然早已被广泛关注,但其上游调控机制仍未被完全阐明。寻找能够从PD-L1上游入手、进而重塑肿瘤免疫微环境的新靶点,正在成为肾癌免疫治疗研究的重要方向。
3月14日,复旦大学生命科学学院王陈继团队和附属肿瘤医院叶定伟/常坤团队在Cell Death & Differentiation发表题为 DPP9 inhibition boosts antitumor immunity by disrupting BRISC-mediated PD-L1 expression in clear cell renal cell carcinoma 的研究论文。该研究发现,DPP9通过扰动BRISC-SHMT2复合体,稳定IFNAR1并激活JAK/STAT-IRF1信号,从而促进PD-L1表达并增强肿瘤免疫逃逸;而药物抑制DPP9后,这一过程可被逆转,肿瘤细胞对T细胞杀伤的抵抗明显下降,抗肿瘤免疫反应得到恢复。
作者首先在小鼠肾癌模型中观察到,DPP9抑制剂1G244在免疫正常小鼠中可显著抑制肿瘤生长,而在免疫缺陷小鼠中作用甚微,提示DPP9主要通过宿主免疫系统发挥促瘤功能。随后,研究进一步通过肿瘤细胞与免疫细胞共培养体系,以及患者来源类器官与免疫细胞共培养实验,证实了DPP9与肿瘤免疫逃逸之间的密切联系。机制上,研究表明DPP9促进肿瘤免疫逃逸主要依赖PD-L1上调。1G244可剂量依赖性地下调PD-L1的mRNA和蛋白水平。进一步实验显示,抗PD-L1抗体基本可抵消Dpp9过表达带来的免疫抑制效应,说明DPP9主要通过PD-L1发挥作用。
在分子机制层面,作者发现DPP9可与SHMT2及BRISC复合体相互作用,并通过扰动SHMT2与BRISC的结合,解除SHMT2对BRISC去泛素化活性的抑制。1G244处理后,这种相互作用减弱,提示该过程依赖DPP9酶活性。进一步研究显示,DPP9可降低IFNAR1的K63连接型泛素化并提高其稳定性,进而激活JAK/STAT-IRF1信号,促进PD-L1表达。敲低BRCC36、敲低IFNAR1或使用JAK1/2抑制剂Ruxolitinib,均可逆转DPP9诱导的PD-L1上调。
在治疗层面,作者进一步测试了DPP9抑制与免疫治疗联用的潜力。结果显示,在免疫正常小鼠模型中,1G244联合抗CTLA-4抗体较任一单药均表现出更强的抑瘤效果,同时可进一步增加CD8? T细胞浸润、降低PD-1阳性耗竭性T细胞比例,并增强IFN-γ和GZMB等效应分子表达。这提示DPP9抑制不仅能够下调PD-L1,还可能通过改善肿瘤免疫微环境,为现有免疫检查点治疗提供增敏作用。
总体而言,这项研究将DPP9明确定位为透明细胞肾癌免疫逃逸的重要调控节点,也提示DPP9小分子抑制有望成为ccRCC联合免疫治疗的新策略(图一)。
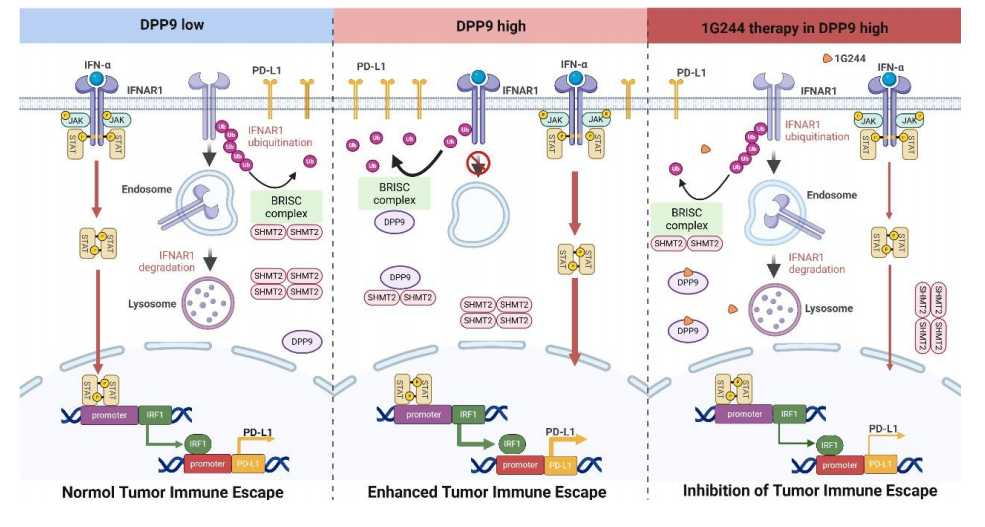
图一 DPP9调控BRISC-SHMT2复合体介导肿瘤免疫逃逸
复旦大学附属肿瘤医院博士后张玮、汪越和博士生冯涛为该论文共同第一作者。王陈继、叶定伟、常坤为论文的共同通讯作者。
原文链接:
https://www.nature.com/articles/s41418-026-01704-x