《Virchows Archiv》:Melanomas arising in blue nevi exhibit absence of TERT promoter mutations, low tumor mutational burden, and high frequency of distant metastases and disease-related mortality: a clinicopathologic and molecular study of 11 cases
编辑推荐:
为解决目前对蓝痣来源黑色素瘤(MBN)的TERT启动子突变(TPM)、肿瘤突变负荷(TMB)及其他分子改变频率认识有限的问题,研究人员对11例MBN开展了全面的临床病理与分子分析。研究发现MBNs具有GNAQ/GNA11突变、无TPMs、低TMB(1突变/Mb)的独特分子谱,并伴有高频率的远处转移(73%)和疾病相关死亡(55%)。该研究丰富了MBN的分子图谱,强调了识别预后因素的重要性,并为其与其它黑色素瘤亚型的鉴别提供了分子依据。
黑色素瘤虽然令人谈之色变,但其家族内成员各异,其中一种罕见且神秘的亚型――“蓝痣来源黑色素瘤”(MBN),因其独特的出身和行为模式,一直是病理学和肿瘤学界关注的焦点。不同于那些与日晒损伤密切相关、常见BRAF或NRAS突变的黑色素瘤,MBN似乎拥有自己的“游戏规则”:它常与GNAQ或GNA11突变相伴,与葡萄膜黑色素瘤的基因特征相似,仿佛披上了一层与众不同的“分子外衣”。然而,这副外衣下的诸多细节仍然模糊。例如,在其它黑色素瘤中常与侵袭性行为相关的TERT启动子突变(TPM),在MBN中是否也存在?其肿瘤突变负荷(TMB)水平如何?除了已知的少数几个驱动基因,是否还存在其他未被发现的分子“帮凶”?更重要的是,这种罕见肿瘤的临床行为究竟有多“恶”?其高转移和高死亡率的传闻是否被数据证实?这些悬而未决的问题,阻碍了临床医生对MBN的精准诊断、预后判断和治疗策略的制定。为此,一项发表于《Virchows Archiv》的研究,通过对11例MBN病例进行深入剖析,试图揭开这层面纱,描绘出更清晰的MBN分子与临床肖像。
为了开展这项研究,研究人员运用了几个关键技术方法。首先,他们从所在三级医院的病理学数据库中筛选出2015至2025年间诊断为MBN、蓝痣样黑色素瘤(BNM)等相关术语的病例。最关键的一步是,他们利用下一代测序(NGS)技术对肿瘤组织进行分子分析。研究中使用了三种经CLIA认证的DNA测序方案,包括靶向50基因、134基因以及更全面的610基因捕获测序面板,从而系统检测了基因突变、拷贝数变异、基因融合、肿瘤突变负荷(TMB)和微卫星不稳定性(MSI)。同时,研究者详细回顾了所有病例的临床病理学特征,包括患者信息、肿瘤组织学形态、免疫组化(IHC)结果(如HMB45, MART-1, PRAME, p16, BAP1, Ki-67等)以及治疗和随访数据,从而将分子特征与临床结局紧密关联。
临床特征与组织病理学特征
研究发现,MBN好发于中年人的头颈部皮肤。所有肿瘤均位于真皮层,呈膨胀性垂直生长,不累及或仅轻微累及表皮,导致诊断时肿瘤厚度中位数高达8.4 mm,所有皮肤来源的MBN均为Clark V级,初始病理分期高。在诊断时,高达64%的病例已出现微观卫星灶(MS)、前哨淋巴结(SLN)阳性或同步转移,这共同导致了较高的初始分期。免疫表型上,MBNs普遍弥漫性表达HMB45和MART-1,60%的病例存在BAP1核表达缺失。值得注意的是,Ki-67增殖指数在不同病例间差异较大,从1-2%到超过20%不等,提示低增殖指数不能单独用于排除恶性肿瘤。
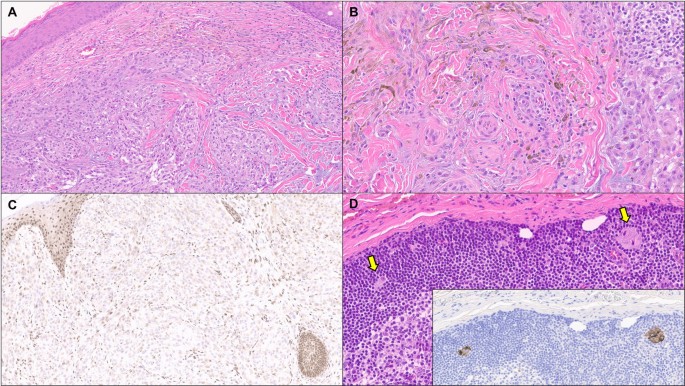
分子特征
分子分析是本研究揭示MBN本质的核心。所有MBN病例(100%)均存在GNA11(64%)或GNAQ(36%)的错义突变,且两者互斥。此外,部分病例还伴有SF3B1(29%)或BAP1(43%)突变。一个关键发现是,所有接受检测的病例(7/7)均不存在TERT启动子突变(TPM)。同时,肿瘤突变负荷(TMB)分析显示MBN具有极低的TMB(三个检测病例均为1突变/Mb),且未发现微卫星不稳定性(MSI)。研究还发现了一些新的分子改变,包括RUNX1T1和SOX17基因的独特扩增,以及TOPBP1和MAP2K1的错义突变,这些改变在MBN中均为首次报道。值得注意的是,在检测的病例中未发现基因融合。
临床随访
在长达36个月(范围3-132个月)的中位随访期内,MBN表现出了极具侵袭性的临床行为。高达73%(8/11)的患者发生了远处转移,最常见部位是肝脏。尽管接受了多线治疗,仍有55%(6/11)的患者死于该疾病,其中一例患者在确诊后仅3个月就因多发远处转移而死亡。研究观察到,存在微观卫星灶(MS)的患者预后似乎更差:在死亡患者中,67%(4/6)存在MS;而没有MS的患者均未死亡,尽管这需要更长时间的随访来验证。
结论与讨论
本研究对11例MBN进行了迄今为止最详尽的临床病理与分子特征描绘之一,并提供了较长的中位随访时间。其结论和重要意义主要体现在以下几个方面:
首先,该研究明确了MBN独特的分子“身份证”:其分子特征以GNAQ/GNA11突变为核心驱动,常伴有SF3B1/BAP1突变,但一致性地缺乏TERT启动子突变(TPM),且肿瘤突变负荷(TMB)极低(1突变/Mb)。这一组合特征将MBN与源于日晒损伤的普通皮肤黑色素瘤清晰地区分开来。尤其重要的是,与另一种在形态上可能与之混淆的亚型――深部穿透性痣样黑色素瘤(DPN-like melanoma)相比,MBN缺乏TPM和低TMB的特征构成了关键的鉴别点,因为后者通常具有高频的TPM和较高的TMB(平均约37突变/Mb)。因此,这项研究为病理诊断,特别是在形态学不典型或存在鉴别诊断困难时,提供了至关重要的分子依据。研究人员指出,不应将TPM状态作为支持或排除黑色素瘤诊断的分子标志物,当鉴别诊断包括MBN和非典型CBN时。
其次,研究扩展了MBN的已知分子图谱,首次报告了RUNX1T1和SOX17基因扩增,以及TOPBP1和MAP2K1错义突变等新的遗传学改变。虽然这些改变在单个病例中出现,其确切的临床意义有待更大规模研究证实,但它们提示MBN的分子机制可能比已知的更为复杂,为未来的机制研究和潜在治疗靶点探索提供了新线索。
最后,研究以详实的数据证实了MBN是一种具有高度侵袭性的恶性肿瘤。高发的远处转移(73%)和疾病相关死亡率(55%),以及诊断时已普遍存在的高肿瘤负荷(中位Breslow厚度8.4 mm)和高病理分期,都突显了早期识别和准确诊断MBN的紧迫性。研究还提示,微观卫星灶(MS)的存在可能与更差的临床结局相关,这或许可作为一个潜在的预后指标。这些发现强调了临床医生和病理学家需要提高对这种罕见但凶险亚型的警惕,其高侵袭性的生物学行为也凸显了开发针对其特定分子通路(如GNAQ/GNA11通路)的有效疗法的必要性。
总而言之,这项研究不仅系统性地描绘了MBN的临床病理与分子全景图,揭示了其无TPM、低TMB的核心分子特征和高转移、高死亡率的侵袭本质,还发现了新的潜在遗传学改变。这些成果深化了我们对这一罕见疾病的认识,为临床精准诊断、预后评估乃至未来靶向治疗的发展奠定了坚实的科学基础。



 生物通微信公众号
生物通微信公众号