��Cancer Immunology, Immunotherapy����Circular RNAs in cancer: Its biogenesis, functions, relationships with cancer progression, applications in immunotherapy and biomarker potentials
�༭�Ƽ���
��������ϵͳ�����˻�״RNA��circRNA���ڰ�֢����������о���չ������������circRNAͨ����ʽ�����γɵĸ߶��ȶ��ṹ��������̽��������ΪmiRNA���ࡢ�뵰���ʻ������䵱֧�ܡ�����ģ�弰����ת¼/����ȶ��ֹ��ܻ��ơ����IJ��־۽���circRNA���ͨ�����ڻ����鲻�ȶ��ԡ�Ѫ�����ɡ�ת�ơ���ϸ�����Ժͻ�����ҩ��������֢��չ����Ϊ��Ҫ���ǣ�����ǰհ�Ե��ܽ���circRNA�ڰ�֢���������еĸ�����Ӧ�ã�����������������ϣ�ICB����Ӧ����Ϊ�¿�ԭ������ȶ�ƽ̨�Լ���������CAR-T�Ʒ����������Ҳ������circRNA��Ϊ�������־��ľ�DZ������ָ���˵�ǰ�о����ٵ���ս��δ��ת������
�������ķ��������У�������һ����̬�����ҹ��ܶ�����RNA���ӡ�����״RNA��circular RNAs�� circRNAs�������Dz�������ʹRNA��mRNA�����������ԣ�����ͨ��һ�ֳ�Ϊ��������ӡ��Ĺ��̣���������3���˺�5���˹������ӣ��γ�һ��û��β�͵ġ���յĻ�״�ṹ����������ġ��ջ�����ƣ�������circRNA�������ȶ��ԣ�ʹ���ܹ��ֿ���������ø�Ľ��⣬�Ӷ���ϸ������Һ�г־ô��ڡ�����������ѧ���Ƿ��֣���Щ�ȶ���circRNA���Ӳ��ǡ����á��ĸ���������ڰ�֢�ķ�������չ�ͶԿ��а����Źؼ���ɫ����Ϊ����������ѧ��������������һ��ȽȽ��������ǡ�
��״RNA�ĵ��������
circRNA������֮��ʼ��ϸ���ˡ�RNA�ۺ�øII��Pol II������ת¼��ǰ����ʹRNA��pre-mRNA������������ԱȾ�������Լ���Ч�ʸ��͵ķ�ʽ���С�������ӡ�����һ�����ε�5������λ����һ�����ε�3������λ�������������Ӷ��γɻ�״�ṹ��Ŀǰ��Ϊ��������Ҫ�ijɻ�ģ�ͣ�һ���ǡ�ֱ�ӷ�����ӡ�����һ�����漰�������м��塱��ģ�ͣ������ֿɷ�Ϊ����������Ծ���͡��ں�����������ȥ��֧�����������͡���������ɳɷ֣�circRNA��Ҫ��Ϊ���ࣺ��ȫ����������ɵ�������circRNA��EcircRNA������ȫ���ں�����ɵ��ں���circRNA��ciRNA���Լ�ͬʱ���������Ӻ��ں��ӵ�������-�ں���circRNA��EIciRNA����
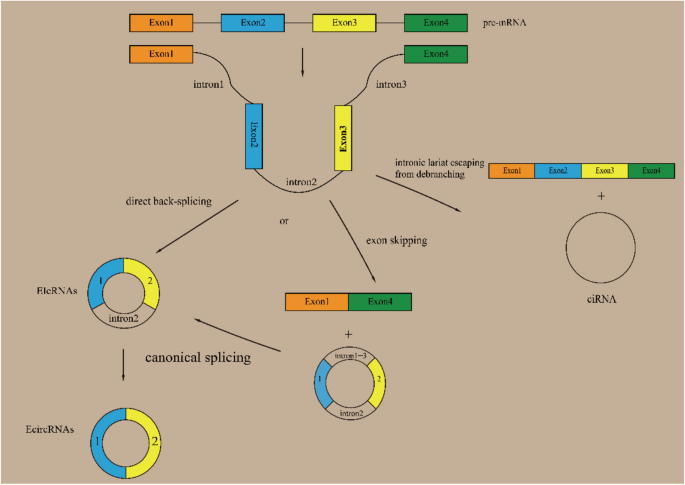
���ܶ�������״RNA�ġ�ʮ�˰����ա�
circRNA֮���Ա��ܹ�ע��Դ��������Ĺ��ܻ��ƣ�ʹ���Ϊϸ���ź������������ĵ�������
- •
�䵱miRNA�������������Ϊ��֪�Ļ��ơ�circRNA�Ϻ�����СRNA��miRNA��������ϵ�λ�㣬��������һ������������Ѻ��miRNA����ֹ��ЩmiRNAȥ�������mRNA�ı���Ӷ�����ϵ��ض�����ı���ˮƽ�����磬circACVR2Aͨ������miR-511-5p�������˺��߶�PIK3CA�����ƣ��Ӷ�����PI3K/Akt�ź�ͨ·���ٽ���ϸ�����Ľ�չ��
- •
�뵰���������������circRNA�ܹ�ֱ�����ض��ĵ����ʽ�ϡ����ֽ�Ͽ����ȶ������ʡ��ı䵰���ʵĻ��ԣ�������ֹ���������뵰���ʽ�ϡ����磬circNFIB�ܹ������Ե���MEK1��ϣ��ƻ�MEK1-ERK2������Ӷ�����ERK�ź�ͨ·���谭���ڵ��ܰ���ת�ơ���һ���棬ȱ���յ���circWSB1�ܹ����ȥ���ػ�øUSP10���谭USP10��p53���Ļ���������p53���ױ����ػ����⣬�Ӷ��ٽ����ٰ��ķ�չ��
- •
�䵱����֧����һЩcircRNAӵ�ж�������ʽ��λ�㣬�ܹ����ּܡ�һ������ͬ�ĵ������ټ���һ�𣬴ٽ������γɹ��ܸ�������磬circPOLR2A����ͬʱ��Ϸ���E3����øUBE3C������ﵰ��PEBP1���ٽ�UBE3C��PEBP1�ķ��ػ����⣬��������ERKͨ·���ƶ�����ϸ�����Ľ�չ��circCDYL2���ܹ��ȶ�GRB7���ף�����ǿ����FAK�Ļ������Ӷ�ά������AKT��ERK1/2ͨ·�Ļ��ԣ��������ٰ��������鵥��������ҩ��
- •
��Ϊ����ģ�������ܴ����circRNA�ǷDZ���ģ������ֺ����ڲ����������λ�㣨IRES����m6A���ε�circRNA��������û��5��ñ�ṹ��������������룬���������Ե�С�Ļ��ʡ����磬circTRIM1���Է������TRIM1-269aa���ף��õ���ͨ����ǿ�Ƶ����ף�CaM��������MARCKSתλ������PI3K/AKT/mTORͨ·���ٽ����������ٰ��Ļ�����ҩ��ת�ơ�circINSIG1������µ������ܴٽ�INSIG1�ķ��ػ����⣬�ر�̽�ֱ�����ĵ��̴���л��
- •
����ת¼�뷭����circRNA����ֱ��Ӱ������ת¼�ͷ�����̡����磬circREEP3������ļȾɫ����������CHD7��FKBP10�������������������ת¼���Ӷ�������ֱ�����Ľ�չ���ڷ�����棬circYap�ܹ����Yap mRNA�Լ�������ʼ����eIF4G��PABP����ֹeIF4G��PABP�������������Ӷ�����Yap���ķ�����ʼ��
������֢���̣���״RNA�ġ����桱��ɫ
��֢�ķ�չ�漰һϵ�и��ӵ���������circRNA�����ֹ㷺��������Щ���̵ĵ��ء�
- •
���ڻ����鲻�ȶ�����ͻ������֢��ʼ�������ǻ���ͻ��Ļ��ۡ��о����֣�circMLL(9,10)����Ⱦɫ���ض�λ���γ�circRNA:DNA�ӽ��壨circR����������ת¼��ͣ�͵���ø�����ơ����ʹ����DNA��¶������ͻ�䣬ͬʱ�����DNA˫������������Ч������������MLL������°���Ⱦɫ����λ���շ���Ѫ�������⣬circNIPBL�ܴٽ��̲��°���NNK�յ���TP53����H179Rͻ����ۣ���circCFL1��ͨ���ȶ�c-Myc�������ٽ�ͻ����TP53�����ת¼����ǿ���������ٰ��ĸ�ϸ�����ԡ�
- •
�ٽ�Ѫ��������������������Ҫ����Ѫ�����ṩӪ����������circRNA�ڴ˹����а����ˡ����֡���ɫ�����磬��ֱ����ϸ���������е�circTUBGCP4����ͨ������miR-146b-3p�ϵ�PDK2������Akt�ź�ͨ·���ٽ�Ѫ����Ƥϸ��Ǩ�ƺͳɹܡ���ȱ�������£�ʳ����״ϸ����ϸ���������е�circ-ZNF609���ͷţ�����Ƥϸ����ȡ��ͨ������miR-150-5p������VEGF-A���ٽ�Ѫ�����ɺ�Ѫ��ͨ�ԣ�Ϊ����ת������ǰת���衱�����������У�EIF4A3�յ�������circ_0059914ͨ������miR-1249�����VEGFA�����ƣ��Ӷ��ٽ�Ѫ�����ɡ�
- •
����ת������������Ϯ��Զ��ת���ǵ�������ʧ�ܺ���������Ҫԭ���о�������circBCAR3��ʳ�ܰ��и߱��ͨ������miR-27a-3p������TNPO1�ı���Ӷ��ٽ���ϸ����ֳ��Ǩ�ơ���Ϯ���������������ڷ�Сϸ���ΰ��У�ȱ���յ�������ϸ�������彫circPLEKHM1���ݸ�����ϸ����circPLEKHM1�ھ���ϸ����ͨ����ǿPABPC1��eIF4G�Ļ������ٽ�OSMR�ķ��룬���յ��¾���ϸ����ٰ���M2�ͼ����������ΰ�ת�ơ�
- •
ά�ָ�ϸ��������������ϸ����������������ҩ��������ת�Ƶĸ�Դ��circKEAP1�����KEAP1-259aa�����ܹ���ϲ��ٽ�Vimentin����ͨ������-����ø��;�����⣬�Ӷ����ƹ������ĸ�ϸ�����ԡ���Ϯ����ֳ���෴��circRREB1��ͨ����YBX1�������������ϸ���ˣ�����WNT7B��ת¼���Ӷ�����Wnt/��-cateninͨ·��ά�����ٵ����ٰ��ĸ�ϸ�����ԡ�
- •
�鵼������ҩ���˷�������ҩ���ٴ��ϵ��ش���ս���о����֣���ɳ������ҩ�Ľ�ֱ����ϸ����ͨ����������ڸ�ˮƽ��circATG4B��������circATG4B-222aa���������ն���һ�������Խ��TMED10����ֹTMED10�����ɵ���ATG4B��ϣ��Ӷ��������ɣ����»�����ҩ�������������ٰ��У�circRNA-CREIT����Ϊ֧�ܵ��ף��ٽ�E3����øHACE1��PKR���ķ��ػ����⣬����Ӧ����������װ��������RACK1/MTK1�����ź�ͨ·���Ӷ���ǿ������ù�ص������ԡ�
���°�֢�������ƣ���״RNA��ȫ����̨
��ͳ�İ�֢�����Ʒ�������������ϣ�ICB����CAR-Tϸ���Ʒ�����Ȼȡ����������Ч������������Ӧ�ʵ͡���ҩ�����õ���ս��circRNA������ص��ȶ��Ժ��ܿ����ԣ�Ϊ��Щ�Ʒ��ĸĽ��ṩ����˼·��
- •
���������������circRNA����Ӱ��ICB�Ʒ���Ч�������磬�ΰ�ϸ���������е�circCCAR1��ֱ�ӽ��Tϸ���ϵ�PD-1���ף���ֹ�䱻���ػ����⣬�Ӷ�ά��PD-1�ĸ߱������CD8+Tϸ�����ܺĽߣ�������PD-1������ҩ���ڷΰ��У�circHMGB2ͨ������miR-181a-5p�ϵ�CARM1�����Ƹ�������Ӧ��ػ���ı���յ������������������������¿�PD-1������ҩ�������ЩcircRNA���и�Ԥ����ʹ�÷���Ѻ������õ�circPIAS1��������������ǿPD-1���Ƽ�����Ч��
- •
����ϸ������������ϸ�����������������йؼ����źŷ��ӡ�circRNA������ض���ϸ�����ӵķ��ڡ��ڽ�ֱ����ģ���У�������circPOLQͨ������IL-10/STAT3�ᣬ�ٽ�����ϸ����M2�ͼ������ڷ�Сϸ���ΰ��У�circNOX4ͨ������miR-329-5p�ϵ�����άϸ������ף�FAP���������յ�IL-6�������ڣ��������Գ���άϸ����̬λ���ٽ�����������ת�ơ�IL-6���������յ�circGGNBP2�IJ�����������cGGNBP2-184aa���������ữ��STAT3��ϣ��γ�IL-6/cGGNBP2-184aa/STAT3��������·����������ٰ��źš�
- •
��Ϊ���Ͱ�֢����ƽ̨�������¿�ԭ��mRNA�����������������Ƶ��ȵ㣬������mRNA�ȶ��ԲcircRNA�ļ����ȶ���ʹ���Ϊ������¿�ԭ�������塣�о������������¿�ԭ��circRNA�����������ܳ�������Ч�ر��ԭ���̼�ǿ�ҵĿ��������߷�Ӧ���������������������ӳ�С�������ڣ���Ч�����ڴ�ͳ������mRNA���硣���⣬�о�������circRNA����Ҳ�������¿�ԭ����Դ���������쳣�Ķ��ܱ�����ϵͳʶ����Ϊ�������廯��circRNA�¿�ԭ����춨�˻�����
- •
��������CAR-T�Ʒ������е�CAR-T�Ʒ����̸��ӡ��ɱ��߰��������ظ����á�����mRNA������˲ʱ����CAR��һ����ǰ�������������������mRNA���ȶ����û�״mRNA��cmRNA���������mRNA�����������ӳ�CAR��Tϸ������ı���ʱ���ǿ�ȡ��о�������װ���˿�CD19-CAR����cmRNA��֬��������������ע����ܰ���Ƣ����������٣�������ԭλ��Tϸ���ر��ΪCAR-Tϸ�������ֻ���cmRNA�ġ�ԭλCAR-T���Ʒ����п��ظ���ҩ����ȫ�Ը��ߡ��Ʊ��������ƣ�Ϊ�������ֻ��͡����ɵ��ص�CAR-T�Ʒ���������·����
�������־���״RNA���ٴ�DZ��
circRNA�㷺�����ڸ�����Һ�У����ڲ�ͬ��������״̬�±��������������ʹ���Ϊ����DZ��������Ϻ�Ԥ�������־�
- •
�����ͨ�����ѪҺ����Һ��������circRNA�ı����ף�����ʵ�ֶ�֢��������Ϻͼ������磬��5��circRNA��ɵļ����ϣ��ܸ߾��ȵ��������ٵ����ٰ������뽡�����գ������ܼ��������ڻ��ߡ��봫ͳ��CA19-9���ã��ɴ��������ȷ�ԣ��ر�����ʶ���CA19-9���Ե����ٰ����ߣ��ֲ������б�־��IJ��㡣���Ƶأ�������circLPAR1��circRNA��ϵ�Ҳ�ڽ�ֱ������θ���ȵ��������ʾ����Խ���ܡ�
- •
Ԥ��������circRNA�ı���ˮƽ�뻼�ߵ�����Ԥ��������ء����磬�ڸ�ϸ�����У��߱���circFOXK2�뻼�߸����Ը��г�������͵��������ʺ���������������أ���Ϊ���ܴٽ��������߲���ЧӦ�������ְ�miRNA�������ٰ�����Ѫ���У�������circPDK1��ˮƽ����������Ϯ���ٴ������Ͳ���Ԥ�������ء���Щ���ֱ�����circRNA������ΪԤ�⼲����չ��ָ�����ƾ��ߵ���Ч���ߡ�
��ս��δ��
����ǰ������������circRNA���о�ת��Ϊ�ٴ�Ӧ�������������ս�����Ƕ�circRNA�ڰ�֢�и��ӵĵ���������֪�Բ�ȫ�棬�����õ�������Ҳ�д����塣��θ�Ч������ؽ�circRNAҩ����͵���ϸ������������ԣ���ؽ������ļ���ƿ����circRNA���еĸ��ȶ���������ʱ�����ƣ�������Ҫ�����书��ʱȴ�����ѵ㡣δ������Ҫ������ؽ���circRNA�Ĺ������磬���������ĵ��ع��ߺ͵���ϵͳ����ͨ���ϸ���ٴ�������֤�䰲ȫ������Ч�ԣ����ս���ŷ�������ľ�DZ��ת��Ϊսʤ��֢������������


