�༭�Ƽ���
������ƪ�����������������ν���ϸ��������֢���Խ�������չ�еĺ��ĵ������ã���Խ���䴫ͳ���Թ��ߡ����ݡ�����ϵͳ�Եز�������ͨ��NF-��B��JAK/STAT3�ȹؼ��ź�ͨ·����Ѫ���ܡ���Ϯǰ�غ�ȱ���������еĿ�����ת�䣬��δ���̬ά����ת��Ϊ���������������ݡ���л֧�ֺ����Ƶֿ��ġ����ס�����������������ʱ��ͼ�ͽ���Һ�����4D�о���ܣ���̽���˰������ν���ϸ��״̬��������siRNA֬�����������Իָ��������Ϲ��ܡ���������/���Ƶġ�״̬��֪����Ԥ�²��ԡ�
���ν���ϸ�����������������ڶ�����
��������ϵͳ�У����ν���ϸ������ḻ�Ľ���ϸ���������ڱ���Ϊ�����Ľṹ֧�š��ִ���ѧ��ʾ�������Ƕ�̬�ĵ����ߣ���ά��������ϵͳ��̬���ɻ�ȱ�IJ��֡����ǹ�����Ѫ�ܵ�Ԫ������ͻ���Ĺؼ����֣�ͨ����������ͷ���������ӡ��ӻ��ᡢѪ��������-1���������ϵ��������ӵ��ף��Ӷ�ά��Ѫ�����ϵ������ԡ����ν���ϸ����ͨ��Ѫ�ܻ��Դ�л�������Ѫ������ͨ���˷�������ת����1��2����Ȱ����Դٽ�������̬��ͨ�����ᴩ�����ԭ�����ṩ��л֧�֣�ͨ��Kir4.1ͨ����������ӵȡ����DZ���Ҳ���ж����ԣ�ԭ���ʺ���ά�����ͱ��ֳ�����ͷ��������ԡ��������������ö��ڽ�����ڲ���״̬�µĿ�����������Ҫ��
���ν���ϸ��������֢�е�����
����֢��������ϵͳ�����ˡ���Ⱦ���ĸ��ӡ�Э���Է�Ӧ�����ν���ϸ�����ڱ���Ϊ������֢������Ӧ��������ϸ��ͬ�ȹؼ���ЧӦ��������λ��Ѫ�����Ϻ㷺ͻ�����ǵ�ս��λ�ã�ʹ���ܹ��䵱Σ���źŵĴ����������߷�Ӧ�ķŴ�����
- •
���ν���ϸ���ļ�������Ϳ�����
���������ϵͳ���ˣ����ν���ϸ��������̵���̬�����Ӻ��ܱ仯��ͳ��Ϊ��Ӧ�����ν���ϸ����������ϸ��ת¼��ѧ��ʾ����Ӧ�����ν���ϸ�����ֳ������ı��Ϳ����ԣ���״̬���ض�����֢����������һ���ؼ��ĸ����ܽ���Ӧ�����ν���ϸ����Ϊ�����ھ���ϸ��M1/M2��������ּ���״̬��A1�����ԣ���A2����������A1������Ҫ��С����ϸ����Դ��ϸ�����ӣ�IL-1����TNF-����C1q���յ����ڴ�״̬�£����ν���ϸ��ʧȥ֧����Ԫ����ͻ��������������ת���������ɱ����Ԫ�ͳ�����ͻ����ϸ���Ķ��Թ��ܡ��෴��ȱѪ���ض����źſ��յ�A2���ͣ�����������Ӫ�����ӣ�����Դ����Ӫ�����ӡ�Ѫ����Ƥ�������ӣ���ѪС�巴Ӧ�����ϵ����Ӷ��ٽ���Ԫ������֯����Ȼ�������ֶ�Ԫģ��Խ��Խ����Ϊ���ȼ���Ӧ�����ν���ϸ���ܿ��ܴ�����һ����ά��ϵ�С��ڽ���ĸϸ�����У��ѻ��ڶ��صĻ��������ʶ�����ͬ�����ν���ϸ�����ͣ�ԭ��������������ͻ����ϸ������Ԫ������Լ���֢�Է�Ӧ�����ν���ϸ�����͡����ֿ�����ͻ�������ν���ϸ�����ܲ��ǹ̶����䣬���Ƕ�̬������֢�������صij���ʱ���ǿ�������졣
- •
�������ν���ϸ���鵼��֢���ź�ͨ·
�Ӿ�Ϣ״̬��Ӧ��״̬��ת�����ض���ϸ�����źż������ء������Ӧ�Bͨ·��Janus��ø/�ź�ת����ת¼��������3ͨ·�����ν���ϸ���鵼��֢����Ҫ�������ӡ�
NF-��Bͨ·�����ν���ϸ���д��׳���ĺ����������ӡ������������£�NF-��B��������I��B��������ϸ�����С�Toll�������ϸ���������壨���ϸ������-1��������������������壩�Ĵ̼�����I��B���⣬����NF-��B��λ��ϸ���ˡ�NF-��B�����ν���ϸ���еļ����ǿЧ�յ��������ӡ�ճ�����Ӻʹ���ϸ�����ӵ�ת¼����ͨ·�������ǽ����ν���ϸ��ת��Ϊ����ЧӦ���������ܰ�ϸ��ļ����������ϵͳʵ���в��Ŵ�ֲ���֢�������ಡ���У���������ĸϸ���������ν���ϸ���������NF-��B������ά��������֢�����Ĺؼ����ơ�
JAK/STAT3ͨ·�Ƿ�Ӧ�����ν���ϸ�������ͽ������γɵ���ҪЭ���ߡ�STAT3���ữ�Ǽ�������������ϵͳ�����з�Ӧ�����ν���ϸ�����ձ��־���ڹ����ϣ�STAT3�źŴٽ����ν���ϸ���ʴ��ϵ�������ά���Ե��ס����ε����м�˿��������Ҫ���ǣ�STAT3���������γɽ�����һ���������ϣ�������֢ϸ���ʹ�Ⱦ�Բ�ԭ�����ɢ���Ӷ������ڽ��Ľ�����֯�����ν���ϸ����STAT3��ȱʧ�ᵼ�¹㷺������ϸ������ͼӾ����Ԫ��ʧ��ͻ�������ڿ�����֢�е���Ҫ���á�Ȼ�����ڰ�֢�����£�ͬһͨ·�ɱ��ٳ��Դٽ��������ơ�
- •
���ν���ϸ��������ϸ�����Ӻ���������
һ����������ν���ϸ����Ϊ����ķ���ϸ�����ͷų������ġ������顱�����Ӱ���ڽ�ϸ������������֢����������������CCL2��CXCL10��CXCL12����Ҫ��Դ��CCL2�ڽ�CCR2+����ϸ����С����ϸ��ļ�������˲�λ�����ر���Ч�����������ݶȶ�����������������ؾ���ϸ���Ļ���Ҳ������Ҫ��ͬʱ�����ν���ϸ������������ϸ������-6��������������-���Ͱ�ϸ������-1�����ڵĴ���ϸ�����ӡ���NF-��B��STAT3���β����İ�ϸ������-6���ж�Ч�����á��������źŴ��������IJ�ͬ���ȴٽ�Tϸ���ֻ���Ҳ֧����Ԫ��Ϊ��������֢�����ν���ϸ��Ҳ�ͷſ���������ת����������-�ºͰ�ϸ������-10����Ȼת����������-��������С����ϸ������������������ϵͳ�������ߵĹؼ����ӣ����ڽ������У����ν���ϸ����Դ��ת����������-��ͨ��������Ȼɱ��ϸ����ϸ������T�ܰ�ϸ������Ϊ�������ݵ�ǿ���������ӡ�
- •
���ν���ϸ����С����ϸ��֮��������
����֢�����ɵ�һϸ���������������Dz��������ν���ϸ����С����ϸ��֮�临�ӵ�˫�����á���С����ϸ�������ν���ϸ�����źŴ����У�С����ϸ��ͨ�������˵ĵ�һ��Ӧ�ߡ��������ϸ���ͷŰ�ϸ������-1����������������-����C1q������Эͬ�����յ�����A1���ν���ϸ�����͡��෴�����ν���ϸ����С����ϸ�����źŴ����������ν���ϸ������С����ϸ��״̬�����Ƿ������-�����ǵ���2�����ӣ�����С����ϸ�����Ǩ�ƣ��Ӷ���ֹ���ȵ�����֢�����ߣ����ν���ϸ���ͷŵ����������ջ�Ȱ�����Լ���С����ϸ�������������壬�Ŵ����߷�Ӧ�������������У����ִ��Ž�����һ������ѭ��������ϸ�����ý���ϸ�������������һ���������Ƶ�������
- •
���ν���ϸ��������֢�е�˫������
���ν���ϸ������֢�е����ñ�������˫�صģ����֡�˫�н���ЧӦ���������³������ڡ������˵ļ����ڣ����ν���ϸ����Ӧ���ںܴ�̶���������ģ�����֯����������Ҫ��������������Ѫ�������Է�ֹˮ�ף���ȡ�˷��Զ��ԹȰ��ᣬ���γɽ������Ը��붾����Ƭ��������֢ϸ����ʵ���ϣ������ڽ���ȫ���ڷ�Ӧ�����ν���ϸ����Ӿ���֯���ˡ�Ȼ���������������£������ķ�Ӧ�����ν���ϸ�����������Ӧ�����������ƻ��ԡ�����ϸ�����ӵij����ͷ�ά����һ�������������Ա�Ķ���ѭ������A1���ν���ϸ����������ͻ���������ͻ����ϸ�����������⣬������б������õĽ����ۣ����ճ�Ϊһ���������������ص����ǵ������ͻ�ѧ���ϣ��谭��ͻ����������ҩ����͡���������˫���ԡ����ڼ����ڵı��������������������µ��к����á����������ƿ���������Ҫ�����������У���ս���Ŵ��ˣ��ٴ�ҽ�������������ν���ϸ������Ĵ��������棬���������Ҫ����̬������ά�ֹ��ܡ�
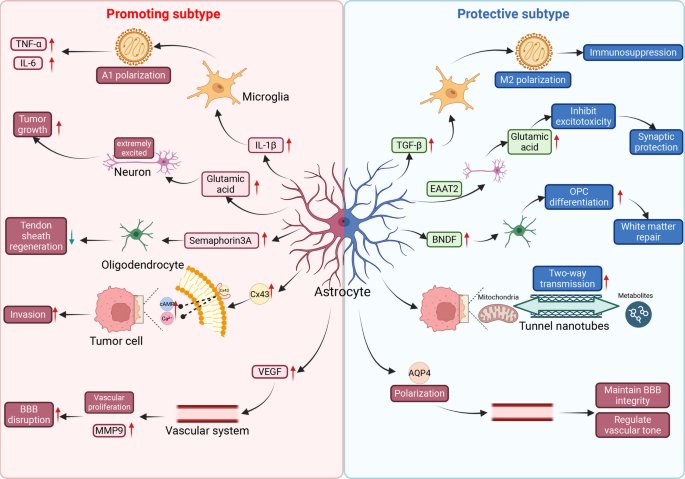
���ν���ϸ������
��Ȼ���ν���ϸ���ڽ�������������̬���ػ��ߣ������ǿ��Ա�в�ȳ�Ϊ��֢��չ�İ��ס��Զ�����������������������һ�����ӵġ����ϵ���̬ϵͳ�����з�Ӧ�����ν���ϸ����������Ϊ����������ν���ϸ���������������ĵ������á�
- •
���ķ���������
����2021������������֯������ϵͳ�������࣬ԭ�����������ķ�����˷�ʽת�䡣��ϵͳ���ȿ��Ƿ��Ӳ������Ǵ�ͳ��֯ѧ���Ӹ����������ˡ����������ķ���ѧ����ǿ����������ϸ������ͻ����ϸ����ϵ��
����ĸϸ������IDHҰ�����dz���������������Ե�ԭ���Զ���������������2021������������֯��������ĸϸ����������ϸ�����IDHҰ���ͺ�H3Ұ���͵�����������ϸ�����������˶����Ե�IDHͻ��ȱʧ�⣬��Щ�������ص��Ǿ����ض��ķ�������������TERT������ͻ�䡢��Ƥ�����������������Լ�7��Ⱦɫ���úϲ�10��Ⱦɫ�嶪ʧ����Щ��ͬ������Ϯ����ֳ�ͻ����鲻�ȶ��ԡ�������ϸ����Դ�����ܽ���ĸϸ����ϸ���������ν���ϸ����־���ϵ���о���������ͨ����Դ��������������ϸ�������Ծ���ȥ�ֻ��Ի�������ν���ϸ������ϸ����״̬����ͻ����ǰ��ϸ�������ٴ���Ϊ�ϣ���Щ����ͨ������������ԭ�������ֳ����ٽ�չ�����������Խ�����ʵ�ʶ����ɱ���ظ�����
����ϸ������IDHͻ��������ǰ����Ϊ���������������Щ����IDH1��IDH2ͻ��ĵͼ���ǰ�������������ڱ�ָ��Ϊ����ϸ������IDHͻ���͡�����ϸ��������ϣ�����ͻ����ϸ������ͬ���������ض��ķ����������壬��ҪIDH1��IDH2ͻ���Լ���ATRX����ȱʧ��/��TP53ͻ�䡣ATRX��һ��Ⱦɫ���������ӣ���ȱʧ���¶�����������ӳ�;������һ�����ϸ�����������ϸ������ϵ��1p/19q��ȱʧ����ͻ����ϸ������IDHͻ���һ���ؼ�������°���л��D-2-�ǻ������IJ������÷��ӱ����ڵ������в�����ΧҰ�������ν���ϸ����ȡ���յ�һ�ֶ��صġ������Ŵ����Ƶı��ͣ���ͬ����IDHҰ���ͽ���ĸϸ�����п����ķ�Ӧ״̬���ٴ��ϣ�IDHͻ����4������ϸ������Ԥ����������IDHҰ���ͽ���ĸϸ����������ԭ�������������е���Щ���������������ν���ϸ�����ֳ��ϵ͵���֢����Ϯ�ԡ�
- •
���ν���ϸ�������������е�����
�������������������ɴ���������ʽṹ����Ķ�����̬λ�������άϸ���������ʵ���Χ������ͬ�����ν���ϸ���Ǵ�������Ҫ�Ļ��ʳɷ֣�ռ��������ϸ��������50%�������������̬ϵͳ�У�����������ν���ϸ�����Ǿ�̬�����DZ��ֳ������Ŀռ������ԡ�
����Ӳ������������еת���ͻ���Ӳ��
�����о�ǿ�����������������������뻯ѧ�ź�ͬ����Ҫ������ĸϸ������֯���Ա�������ʵ�ʸ���Ӳ����Ӧ�����ν���ϸ��ͨ������ϸ������ʵ��ף������쵰��-C���������������ᣩ������Ӳ���Ĺؼ������ߡ����ν���ϸ��ͨ����е����ͨ���������������֪�������ӵ�Ӳ�ȡ���Щ�������ļ����ת¼����������YAP/TAZ�ĺ�תλ�����һ���Ŵ������ν���ϸ���еĴ���������ʱ��͡���Ͳ�����һ��ǰ��ѭ��������Ӳ���������ν���ϸ�� �� ��������ν���ϸ�����ڸ���ϸ������� �� ������ø���Ӳ��������Ϯ�ԡ�
�ռ������ԣ���ͬ�Ĺ�����̬λ
����������ν���ϸ���Ĺ��ܴܺ�̶���ȡ����������������ſ�Ŀռ�λ�á���ȱ�����������ģ����ν���ϸ��ͨ��ϡ�ٻ��˻�������Ⱥ�壬����Ϊ�������-ȱ�������ν���ϸ������л����Ӧ�ǽͽ⣬��Ѫ����Ƥ�������ӵ���Ҫ��Դ����������ĸϸ���������Ե�����Ѫ�����ɡ���Ѫ������̬λ��Ѫ�������ν���ϸ������Ѫ�������ϵ�ά��������Ҫ���ڸ��������У�Ѫ�������ν���ϸ��������Ѫ�ܱڵIJ����Ի�������ʧȥ������ˮͨ������4������¡�Ѫ�ܽ����Ѫ�������ƻ����������Ϯǰ�أ���Ӧ�����ν���ϸ������γ�һ��ּ�����������ġ��������ơ��߽硣Ȼ��������ĸϸ�������ڵ��������ա���������Щ���ν���ϸ��������Ӷ�������ת��Ϊ�ٽ���������ϸ���ذ����������Խ����֧�ܡ�
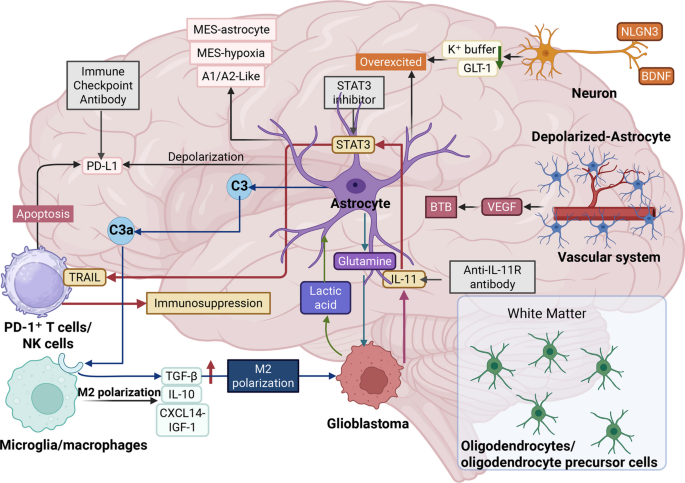
- •
���ν���ϸ����������Ϯ����ֳ��ת�Ƶ�Ӱ��
����ϸ��������������ν���ϸ��֮�����������������ı�־���������ⲻ��һ��������֧��ϵͳ������һ�������ġ�˫��ĺ����������˴��Ե������ʹ�л���ۡ�
������Ϯ��ϸ������ʺ����ӵ�������
����ĸϸ������������֪����Ϯ������������������ν���ϸ��ͨ�����ַ��ӻ��ƴٽ����ֽ������ȣ���Ӧ�����ν���ϸ���Dz���������ܵ�ø���ر��ǻ��ʽ�������ø2�ͻ��ʽ�������ø9���Ķ�������ߡ���Щø����ϸ������ʳɷ֣���Ч��Ϊ����ϸ�����������Ǩ�Ƹ��ٹ�·�������⣬���ν���ϸ�������쵰��-C�ϵ�������ϸ���еĻ��ʽ�������ø12����һ���Ŵ���Ϯ��������Σ�ͨ�����ӵ���43��϶���ӽ���ֱ�������Ӵ�������ż��ʹ���źŷ��ӣ������Ϯ��С���Ǻ��ᣩ�ܹ��ڽ���ĸϸ����ϸ�������ν���ϸ��֮��˫��ת�ơ���������������Դ���ź��£����ν���ϸ�����Ծ��������ת���������ˮƽ�IJ��ε������쵰��-C������״̬֧�������ġ�ǰ�ء�����������������ϸ���ذ�����Ǩ�ơ�������о������ǿ���˽���ϸ��ճ�����ӵ����ã����ڽ���ĸϸ���������ʱ���߽���ϸ��ճ�����ӱ���ٽ��������ĵ�ϸ��-ϸ��ճ������ֳ�����ͱ���������ǿ��ʵ�ʺ�Ѫ����Ϯ��ء�
�ٽ���ֳ����л��ϸ����֧��
���ν���ϸ���䵱��л��Ŧ����һ���������������б�Ų����Ϊ�������������ṩȼ�ϡ���һ�����˵�ϸ�����ٳ������У�����ĸϸ����ϸ�����ڽ������ν���ϸ���γ��������ܡ�ͨ����Щͨ�������ν���ϸ���������Ե�������ת�Ƹ�����ĸϸ����ϸ������ǿ���������������ữ��������������ֿ���лѹ������������һ����ͨ��������Ӧ���ͻ����ϵ�������ϸ����ת�ƣ�����������ν���ϸ����ͨ����лż��֧��������л�����ν���ϸ���ϵ��Ȱ�����ת���壬�������-˿����-���װ���ת����2������Ϊ����������ϳɵĵ�Դ����ȱ���������ˡ����ᴩ�����ν���ϸ��ͨ��������ת�˵���1��4������ᣬͨ������WarburgЧӦ֧���������������յIJ�����������о���һ����ʾ����Ԫ������ٽ���������������յ��ġ���������-��������ø10�鵼�������ӵ���3���䣬����Դ����Ӫ������һ����Ϊ���������ӣ�ͨ����-����-3-�ǻ�-5-��-4-�����������鵼�ĵ�������������ϸ����ֳ��
��ת�Ƶ����
���ڼ̷��������������ν���ϸ����������ʱ���ݱ䣬���ֳ�һ����ۡ��ڳ�ʼת�ƶ�ֲʱ����Ӧ�����ν���ϸ����������ã����ǰ�Χת����ͷ�����øԭ���������������ø���յ���ϸ����������һ�δ����˶�ֲ��һ����Ҫƿ����Ȼ�������İ�ϸ�����ս����ν���ϸ���ر��Ϊ֧���ԡ���ת�Ƶ�״̬����Щ��Ų�õ����ν���ϸ���µ�����øԭ��������Ƽ������������ϸ������-6����Դ����Ӫ�����ӵȴ�����ӣ�����ת���������ܻ���Ӱ�졣��ʶ����ض����ƣ����磬�ڷΰ���ת���У����ν���ϸ������Wnt5a����ٽ��˰�ϸ���д�л�Ȱ�������1�ı�����д�л�Ȱ�������1���Ƥ��������������������ò�ʹ���ȶ����Ӷ���ǿ���ε�ϸ�����źŵ��ڼ�ø�źŴ����������ٽ���ϸ������ֳ�ʹ�
- •
���ν���ϸ�����������ݵĹ���
����������ν���ϸ����ؼ�������֮һ������һ������ѧ�ϵġ��䡱����������������ν���ϸ��ͨ���ض��ķ��Ӽ����ϸ���������������ǿ�����Ե�������Ȩ��
��ϸ������-11/TNF��ص����յ����������
���ν���ϸ���鵼���������Ƶ�һ���ؼ������漰������Tϸ�����������ĸϸ����ϸ�����ڰ�ϸ������-11���������ν���ϸ���ϵ������ϣ������ź�ת����ת¼��������3ͨ·���ź�ת����ת¼��������3�ļ����յ����ν���ϸ������TNF��ص����յ����塣�������ν���ϸ����Դ��TNF��ص����յ����������Tϸ���ϵ����������ϣ���������������ֻ�����Ч����������Χ������һ����ɱ�������������˿���������ϸ����
��������������-����1������������
����������ν���ϸ�������������г�������������-����1����Ҫ��Դ���ڸ�����-�ºͰ�ϸ������-10���źŵ������£����ν���ϸ���ϵ������������������-����1�ı����������������-����1������ϸ������T�ܰ�ϸ���ϵij�������������1��ϣ��յ�Tϸ���Ľߺ�ʧ�ܡ����ν���ϸ�������ϳ�������������-����1��TNF��ص����յ��������ϱ�����������ƹ�����һ��ǿ������ϡ�
ϸ������Э���;���ϸ������
����������ν���ϸ��ͨ������ת����������-�ºͰ�ϸ������-10��ά���������ƻ�����ת����������-����Ϊ���������ӣ�������Ȼɱ��ϸ�����Բ����ϸ������T�ܰ�ϸ����ֳ�����ν���ϸ��Ҳ������CCL2�ͼ���̼�����1�����������Դ�����ļ������ϸ���������������У����ν���ϸ����Դ��ת����������-�ºͰ�ϸ������-10����Щϸ������ΪM2��������ؾ���ϸ������һ���������߷�Ӧ��֧��Ѫ�����ɡ�
ͨ�����ν���ϸ�����е�����֢����֮��Ľ�������
����֢����֮��Ĺ�ϵ����������صģ������������֯�ģ����ν���ϸ���Ǵٽ����ִ��ŵ������ź���Ŧ�������������У����˿����ϡ���Ӧ�͡�������������֮���������ģ��������ϸ���ٳ��˱��ص���֢ͨ·�����ر�����ν���ϸ�������������̬�ķ�����ת��Ϊ���������Ļ��������ߡ�
- •
���ν���ϸ���ı����Ŵ���ȱ���ر��
���������е����ν���ϸ��������һ���ಽ����̣����Է����źš���лӦ��Դ��ȫ������״̬�����������з��п����ļ������ν���ϸ��������ͬ��������������



