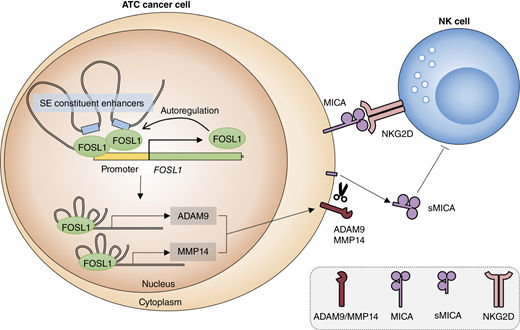
ժҪ
δ�ֻ���״�ٰ���ATC���������Ϯ�Եļ�״�ٰ����ͣ����������ڽ�Ϊ7��10���¡���ǰ���о�������ATC����������TME���е���Ȼɱ��ϸ����NKϸ��������������ϸ�����Խ��͡��������о��У�����̽���˳�����ǿ�ӣ�SE��������ATC TME�е����ã�������ǿ����һ�����ڵ���ǿ�ӣ��ܹ���������ĸ߱����ATC�г�����ǿ�Ӿ��۵�ȫ�������ʾ���°�������ǿ�ӵļ����ǵ��¼�״�ٰ�ȥ�ֻ���δ�ֻ�ת���Ļ��ơ�����ATC�з������ֵij�����ǿ�ӵ��������뻼���������������������йء�FOSL1��ȷ��Ϊһ���ɳ�����ǿ��������ת¼���ӣ���ATCϸ���ı����Ŵ�����������Ҫ����Ȥ���ǣ�FOSL1���������ij�����ǿ�ӽ�ϣ��ٽ���Ⱦɫ�ʻ�����Զ����ǿ������������֮��Ŀռ��ڽ��ԣ���ά������߱���γ���һ�����������ҵ��ڻ�·����ATC��չ�����У�FOSL1ͨ�����䳬����ǿ�ӵĽ����ǿ�˽�������øADAM9��MMP14�ı����ٽ���MICA��ϸ����������䣬�Ӷ�����ϸ���ӱ�NKϸ����ɱ�ˡ�������ʵ���У���ĬFOSL1��ADAM9��MMP9������ATCϸ����NKϸ��ɱ�˵������ԣ���������ʵ���У���Щ��Ĭ����������ATC����������Щ���ֹ�ͬǿ����FOSL1��ATCȾɫ�������Լ�����NKϸ��ϸ�����Թ����е����ã��Ӷ�ΪDZ�ڵİ�֢���Ʒ����ṩ�˼��⡣
�Ե��¼�״�ٰ�ȥ�ֻ���δ�ֻ�ת�����°�������ǿ�ӵķ���������FOSL1�DZ����Ŵ����ܺ��������ݵ��������أ���ͻ���˰���FOSL1��δ�ֻ���״�ٰ������е�DZ����
ͼ��ժҪ
 ����ͨ�Ź��ں�
����ͨ�Ź��ں�
 ����ͨ������
����ͨ������