
-

生物通官微
陪你抓住生命科技
跳动的脉搏
【科研动态】肠道菌群和代谢物的多组学挖掘,揭示治疗儿童脓毒症新策略:肠道共生菌来源胆汁...
【字体: 大 中 小 】 时间:2026年05月07日 来源:华中科技大学生命与科学技术学院
编辑推荐:
2026年5月1日,华中科技大学生命科学与技术学院宁康教授、刘欣教授团队联合武汉纺织大学朱泉霏教授、冯钰锜教授团队,在《Nature Microbiology》发表研究论文,系统揭示了儿科脓毒症中的“肠道菌群—胆汁酸轴”调控机制
2026年5月1日,华中科技大学生命科学与技术学院宁康教授、刘欣教授团队联合武汉纺织大学朱泉霏教授、冯钰锜教授团队,在《Nature Microbiology》发表研究论文,系统揭示了儿科脓毒症中的“肠道菌群—胆汁酸轴”调控机制。研究团队通过整合临床队列多组学分析、小鼠模型验证以及肠道类器官功能实验,发现肠道共生菌棉子糖肠球菌(Enterococcus raffinosus)可产生一种关键硫酸化胆汁酸——脱氧胆酸3-硫酸酯(DCA-3S),该代谢物能够通过激活法尼醇X受体(FXR),改善肠屏障功能、减轻炎症反应,并缓解脓毒症进程。这一发现不仅为儿童脓毒症提供了新的诊断标志物,也为基于微生物代谢物的精准干预策略提供了新方向。
迫切的临床研究背景
脓毒症是儿童重症监护领域长期面临的重要挑战。全球每年约有超过2000万五岁以下儿童受到脓毒症影响,其死亡率始终居高不下。虽然抗感染治疗和器官支持手段不断进步,但传统治疗方式往往难以恢复肠道菌群失衡及肠屏障破坏所引发的系统性炎症恶化。越来越多研究提示,肠道不仅是感染的重要源头,更是调控免疫稳态和炎症进展的关键器官。然而,在儿童脓毒症背景下,肠道菌群如何通过代谢物影响疾病发展,仍缺乏系统认识。
从肠道菌群与胆汁酸“对话”中寻找关键线索
为揭示儿童脓毒症中的代谢调控机制,研究团队招募165名儿科脓毒症患者及健康对照,通过靶向代谢组学分析99种胆汁酸及其修饰形式,构建胆汁酸谱图。结果显示,脓毒症患儿胆汁酸组成显著异常,其中脱氧胆酸3-硫酸酯(DCA-3S)水平明显升高。机器学习分析表明,DCA-3S具有较强的疾病识别能力,并在独立验证队列中保持稳定诊断性能。此外,DCA-3S与多项炎症指标显著相关,提示其不仅可作为诊断标志物,还可能参与脓毒症病理调控。
推翻传统认知:肠道菌群是DCA-3S的主要来源
长期以来,胆汁酸硫酸化被认为主要由肝脏完成。然而,本研究提出了新的观点:肠道菌群同样具备产生硫酸化胆汁酸的能力。通过菌株筛选、稳定同位素示踪及小鼠代谢追踪,研究团队证实棉子糖肠球菌(Enterococcus raffinosus)是DCA-3S的重要来源,其在体内贡献超过80%,而肝脏作用有限。空间分布分析进一步显示,DCA-3S主要存在于回肠、盲肠和结肠等菌群丰富区域,在肝脏和胆囊中几乎检测不到。这一发现挑战了“肝脏主导胆汁酸硫酸化”的传统观点,揭示了肠道微生物在胆汁酸修饰中的关键角色。
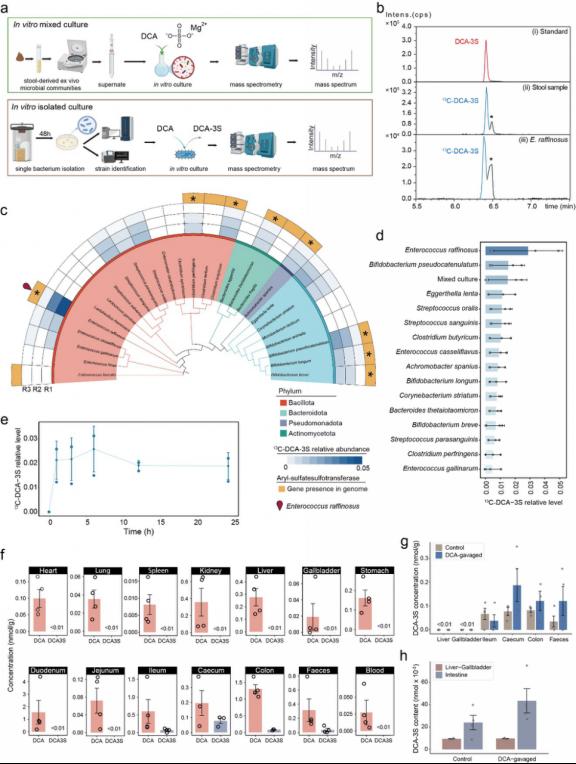
图1. 多组学数据挖掘,揭示DCA-3S的菌源性
DCA-3S重塑肠屏障并减轻炎症反应
为验证DCA-3S的生物学作用,研究团队进一步开展了脓毒症小鼠和肠道类器官实验。结果显示,无论预防性还是治疗性给药,DCA-3S均可显著降低炎症指标,减轻肠道病理损伤,改善肠绒毛结构并减少炎性细胞浸润。在脓毒症来源的肠道类器官中,DCA-3S可降低上皮通透性、增强紧密连接蛋白表达,同时抑制细胞凋亡,促进肠上皮细胞增殖与分化,加速肠屏障修复。此外,DCA-3S还能部分恢复受损菌群多样性,促进有益菌增殖。
机制研究表明,DCA-3S可直接结合并激活法尼醇X受体(FXR),该受体参与胆汁酸代谢及肠道稳态维持。在FXR缺陷小鼠中,DCA-3S的抗炎及肠屏障修复作用完全消失,说明FXR是其关键作用通路。结果提示DCA-3S不仅是代谢产物,更是具有明确生理功能的内源性信号分子。
该研究首次系统揭示了儿科脓毒症中的“肠道菌群—胆汁酸—FXR”调控轴,提出DCA-3S作为关键微生物代谢物,在疾病发生发展中发挥双重作用:既可作为高敏感度的诊断标志物,也可作为潜在治疗分子改善肠屏障和炎症状态。与传统抗生素治疗不同,DCA-3S属于人体内源性代谢产物,具有较好的生物相容性和低毒性优势,其较高的水溶性也降低了胆汁酸对细胞膜的潜在损伤风险。
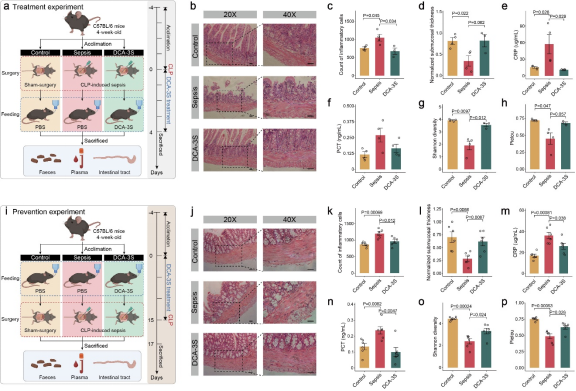
图2. 治疗模型和预防模型的实验,共同验证了DCA-3S改善肠屏障功能的作用
这项工作不仅拓展了对脓毒症机制的理解,也为“以菌养肠、以内源代谢物调控宿主防御”的精准治疗理念提供了新的实验依据。未来,围绕微生物代谢物开展的诊断与治疗研究,有望为儿童脓毒症的早期干预和个体化治疗带来新的突破。
华中科技大学生命科学与技术学院宁康教授、刘欣教授团队,武汉纺织大学朱泉霏教授、冯钰锜教授团队,为本文共同通讯作者。华中科技大学、武汉大学、武汉纺织大学的硕博士研究生刘翔、张浩博、王彦真、涂欣雨、文杰杰,为论文共同第一作者。该研究得到了国家重点研发计划和国家自然科学基金等项目的资助。
文章链接:https://doi.org/10.1038/s41564-026-02351-1