
-

生物通官微
陪你抓住生命科技
跳动的脉搏
汪胜组和丛尧组合作开发孤儿受体结构解析新策略
【字体: 大 中 小 】 时间:2026年05月08日 来源:中国科学院生物化学与细胞生物学研究所
编辑推荐:
5月5日,国际学术期刊PNAS在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)汪胜研究组和丛尧研究组联合中山大学李典范教授及国科大杭高院生命学院樊鲁玉博士的合作研究成果:“Decoding the Structure of GPR151 via NELiS”
5月5日,国际学术期刊PNAS在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)汪胜研究组和丛尧研究组联合中山大学李典范教授及国科大杭高院生命学院樊鲁玉博士的合作研究成果:“Decoding the Structure of GPR151 via NELiS”。研究团队针对长期困扰领域的“孤儿受体”结构解析难题,提出了一种全新策略,并首次解析了孤儿受体GPR151(高度集中表达在与负性情绪密切相关的大脑缰核区域)的高分辨率冷冻电镜结构,为该类重要药物靶点的系统性研究打开突破口。
G蛋白偶联受体(GPCR)是人体内规模最大、分布最广泛的膜蛋白超家族之一,约三分之一的上市药物均以其为靶点。然而,在这一庞大体系中,仍有超过140种GPCR因缺乏明确的内源性配体而被称为“孤儿受体”。它们广泛存在于中枢神经系统,与焦虑、抑郁及神经退行性疾病密切相关,却因“无配体、无效应蛋白”的双重缺失,长期难以解析其结构与功能,被形象地称为“无钥之锁”。
围绕这一核心瓶颈,研究团队首先利用纳米抗体Nb6构建“分子支架”,通过工程化改造使孤儿受体能够被稳定“锁定”在特定构象。进一步地,团队发展出一种无需配体、无需纯化蛋白的热稳定性突变筛选策略――NELiS(Nb6-Enabled Ligand-Free Stabilization Platform)。该方法突破传统依赖配体或纯化体系的限制,仅通过细胞粗提物即可快速筛选稳定突变,大幅降低实验门槛并显著提升效率。借助NELiS,研究人员在GPR151中成功识别出4个关键热稳定突变,并获得稳定的受体复合物,最终成功解析了GPR151的非激活态冷冻电镜结构。
结构结果揭示了GPR151一系列“反常规”的分子特征:其经典激活开关W6.48呈异常“向上翻转”构象,并被多重极性相互作用锁定;关键结构基序由疏水环境转变为更亲水配置;Na+结合位点及离子锁结构也发生系统性重塑。这些改变共同提高了受体激活的能垒,使GPR151稳定维持在非激活状态。
更引人关注的是,研究发现GPR151的N端如同“内置闸门”,直接插入配体结合口袋上方,物理性阻断潜在配体进入;当移除这一结构后,受体呈现出更接近肽类GPCR的开放构象,并表现出激活趋势。这一发现提示,GPR151可能依赖一种区别于经典GPCR的全新调控机制。
结合其在脑内缰核―脚间核通路中的独特突触前定位,研究团队提出:GPR151可能并不依赖传统“配体―受体―效应蛋白”模式,而采用更加特殊的信号调控方式。这一发现不仅拓展了人们对GPCR作用机制的认知,也为理解神经精神疾病提供了新的分子视角。
总体而言,本研究发展了可推广的孤儿GPCR结构解析新范式NELiS,并首次揭示GPR151的结构基础,为后续功能研究及药物开发奠定了关键基础。该策略有望加速一大类“沉默靶点”的系统性解锁。
分子细胞卓越中心汪胜研究员、丛尧研究员,中山大学李典范教授及国科大杭高院生命学院樊鲁玉博士为论文的共同通讯作者。分子细胞卓越中心博士研究生王雨朦,国科大杭高院生命学院樊鲁玉博士,分子细胞卓越中心博士研究生宋千千、李雅宁为本文共同第一作者。感谢国家蛋白质科学研究(上海)设施冷冻电镜系统、数据库与计算分析系统的大力支持。该研究得到了国家自然科学基金、科技部重点研发项目、中国科学院战略先导研究项目等项目的支持。该研究获得分子细胞卓越中心细胞分析技术平台、分子生物学技术平台给予的支持。
文章链接:https://doi.org/10.1073/pnas.2534234123
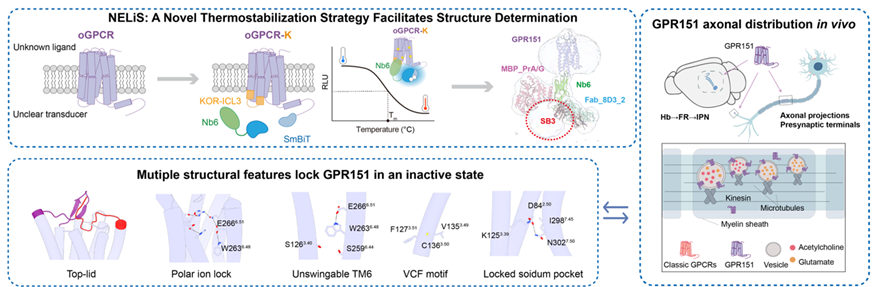
NELiS助力孤儿受体GPR151的结构解析